Антибактериальная терапия внебольничной пневмонии 2015

СОДЕРЖАНИЕ
ОБЩИЕ СВЕДЕНИЯ
ВАЖНО ЗНАТЬ
ТАКТИКА И СТРАТЕГИЯ ЛЕЧЕНИЯ ПНЕВМОНИИ У ВЗРОСЛЫХ
ЛЕЧЕНИЕ ПНЕВМОНИИ В СТАЦИОНАРЕ
ЗАКЛЮЧЕНИЕ
Внебольничная пневмония (синонимы: домашняя пневмония, амбулаторная, воспаление легких) — это острое инфекционное заболевание легких, возникшее во внебольничных условиях или в первые 48 часов госпитализации, сопровождающееся симптомами инфекции нижних дыхательных путей (температура, кашель, боли в груди, одышка) и «свежими» очагово-инфильтративными изменениями в легких при отсутствии очевидной диагностической альтернативы. Внебольничная пневмония у взрослых (воспаление легких у взрослых) довольно распространена. По результатам современных эпидемиологических исследований, заболеваемость внебольничной пневмонией у взрослых составляет 3-40%, около 50% из них госпитализируются. При этом каждый 10-й пациент с внебольничной пневмонией в силу тяжелого или осложненного течения заболевания помещается в отделение интенсивной терапии (ОИТ). И если летальность среди амбулаторных больных, как правило, не превышает 0,5 %, то госпитальная летальность достигает 14 % и более.
Согласно данным официальной статистики, заболеваемость пневмонией в РФ в 2018 г. составила 490,6 на 100 тыс., что на 19 % превысило аналогичный показатель, зарегистрированный в 2017 г. (412,3/100 000); отмечен также и рост летальности (на 2,2 %) больных внебольничной пневмонией – с 19,11/100 000 в 2017 г. до 19,8/100 000 в 2018 г.
При этом ведущее место в достижении оптимального исхода у данной категории пациентов занимает своевременно начатая рациональная антибактериальная терапия (АБТ).
Основные вопросы, связанные с антибактериальной терапией (антибиотики при пневмонии):
I. Стратификация пациентов. При выборе антибиотика нужно учитывать факторы риска неблагоприятного исхода и степень тяжести заболевания. Также следует принять во внимание наличие известных факторов риска появления отдельных возбудителей внебольничной пневмонии у взрослых – лекарственноустойчивых Streptococcus pneumoniae 1*, грамотрицательных энтеробактерий *2, Pseudomonas aeruginosa *3.
1*Возраст > 65 лет, терапия β-лактамами в течение последних 3 мес, множественные сопутствующие заболевания внутренних органов (сахарный диабет, сердечная недостаточность, ХОБЛ и др.) и др.
2*Обитатели домов престарелых, проводимая антибактериальная терапия, множественные сопутствующие заболевания и др.
3*«Структурные» заболевания легких (например, бронхоэктазия), системная терапия глюкокортикоидами, упадок питания, терапия антибиотиками широкого спектра действия более 7 дней в течение последнего месяца.
II. Соотношение «цена/эффективность». Идеальный антибиотик – это не самый дешевый препарат. Оценивая прямые затраты на лечение (прежде всего, в амбулаторных условиях), со стоимостью лекарственного средства нужно соотнести длительность нетрудоспособности пациента и частоту терапевтических неудач, в том числе повлекших за собой госпитализацию. Разумеется, что стоимость антибактериальной терапии зачастую несопоставима с последствиями терапевтической неудачи.
III. Приверженность пациента лечебным рекомендациям. Серьезными препятствиями к выполнению пациентом назначений являются: обилие и частота приема лекарственных препаратов, влияние лечения на сложившийся жизненный стереотип и минимальные последствия несоблюдения врачебных рекомендаций в представлении больного.
При решении этих и других вопросов, связанных с антибактериальной терапией, нужно учитывать следующее:
а) традиционные диагностические тесты, направленные на этиологическую верификацию ВП, характеризуются ограниченной ценностью (их результативность не превышает 50 %);
б) антибактериальная терапия пневмонии, по крайней мере в дебюте заболевания, носит эмпирический характер;
в) выбор и время начала АБТ имеют определяющее прогностическое значение;
г) ключевыми возбудителями большинства случаев внебольничной пневмонии являются Streptococcus pneumoniae (пневмококк), Haemophilus influenzae, «атипичные» микроорганизмы (Chlamydophila pneumoniae, Mycoplasma pneumoniae);
д) доказан реальный вклад коинфекции (например, сочетании пневмококка и «атипичных» возбудителей) в развитие внебольничной пневмонии;
е) все более актуальной становится проблема распространения лекарственноустойчивых штаммов основных возбудителей внебольничной пневмонии.
В целом же выбор обоснованной эмпирической антибактериальной терапии внебольничной пневмонии строится на знании ограниченного перечня возбудителей заболевания и предсказуемых уровней резистентности в пределах обширных географических регионов. Так, к числу основных возбудителей внебольничной пневмонией нетяжелого течения, т. е. не требующей госпитализации, относятся S. pneumoniae, M. pneumoniae, C. pneumoniae, тогда как среди микробиологических «находок» у больных с более тяжелым течением заболевания, нуждающихся в госпитализации (в т. ч. в ОИТ), наряду с пневмококком, H. influenzae фигурируют Legionella pneumophila, представители семейства Enterobacteriaceae (прежде всего, Klebsiella pneumoniae, Escherichia coli), Staphylococcus aureus.
В выборе рациональной антибактериальной терапии, помимо ориентированности в этиологии ВП, не менее важно знать структуру лекарственной устойчивости ключевых возбудителей заболевания, и, прежде всего, пневмококка. В некоторых странах устойчивость пневмококков к пенициллину достигает 60 %, причем многие из них обладают резистентностью к трем и более классам антибиотиков. Резистентность S. pneumoniae к пенициллину обычно сочетается с устойчивостью к цефалоспоринам I–II поколений, тетрациклинам, ко-тримоксазолу.
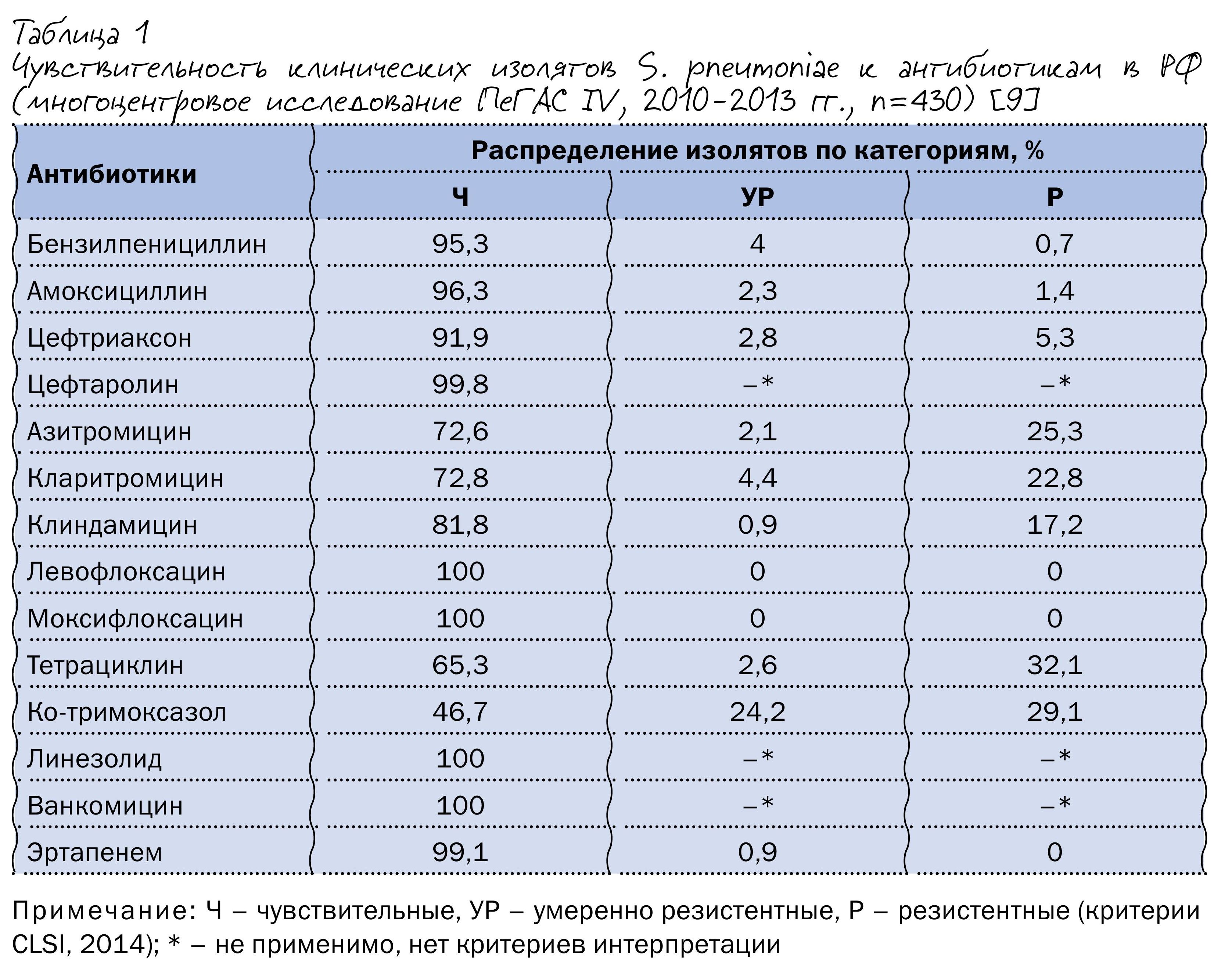
Данные мониторинга чувствительности клинических штаммов S. pneumoniae в РФ, выделенных у пациентов с внебольничными инфекциями нижних дыхательных путей в 2010–2013 гг., представлены в таблице 1. Отличительная черта нашей страны – высокий уровень резистентности пневмококка к тетрациклинам и ко-тримоксазолу, что может быть связано с неоправданно высокой частотой их применения в XX – начале XXI вв. Уровень же устойчивости S. pneumoniae к пенициллину и аминопенициллинам остается относительно невысоким – 4,7 и 1,4 % изолятов соответственно.
Резистентность пневмококка к различным макролидам и линкозамидам варьирует в пределах 18–27,4 %; большинство макролидорезистентных пневмококков демонстрируют устойчивость к клиндамицину, что может свидетельствовать о преобладании в РФ MLSB-фенотипа резистентности, обусловленного модификацией мишени и определяющего устойчивость S. pneumoniae ко всем макролидам, включая 16-членные.
В настоящее время появились доказательства превосходства некоторых подходов к лечению взрослых больных ВП. Так, целесообразность раннего назначения антибиотиков (в первые 4–8 ч от момента госпитализации) подтверждаются результатами обсервационных исследований и согласуется с мнением экспертов.
Для снижения затрат можно использовать современные рекомендации, облегчающие выбор пациентов ВП, которые могли бы безопасно и эффективно лечиться в амбулаторных условиях.
По возможности ранний переход с парентерального введения антибиотика на его прием внутрь и следующая за этим выписка из стационара (когда пациент становится клинически стабильным) также снижает стоимости лечения.
Выбор препаратов для стартовой антибактериальной терапии больных внебольничной пневмонией определяет спектр потенциальных возбудителей заболевания и профиль антибиотикорезистентности. При этом важно иметь в виду, что «…данные, полученные из существующих рандомизированных клинических исследований, не позволяют создать доказательные рекомендации по выбору антибиотика для терапии внебольничной пневмонии». Поэтому стратификация больных и рекомендации по выбору антибактериальной пневмонии в большей степени отражают национальные эпидемиологические данные антибиотикорезистентности ключевых возбудителей внебольничной пневмонии, их потенциальное экологическое влияние, а также учитывают затратную эффективность лекарственной терапии.
Согласно положениям проекта национальных рекомендаций, подготовленных экспертами Российского респираторного общества (РРО) и Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии (МАКМАХ), среди больных пневмонией, которые могут получать лечение в амбулаторных условиях, целесообразно выделять 2 группы. В первую из них включены пациенты без серьезных хронических заболеваний внутренних органов, не принимавшие за последние 3 мес системные антибиотики и не имеющие другие факторы риска инфицирования редкими и/или полирезистентными возбудителями (пребывание в доме престарелых или других учреждениях длительного ухода, наличие госпитализаций по любому поводу в течение ≥2 суток в предшествующие 90 дней, в/в инфузионная терапия, лечение ран в домашних условиях в предшествующие 30 дней и др.) (рис. 1).
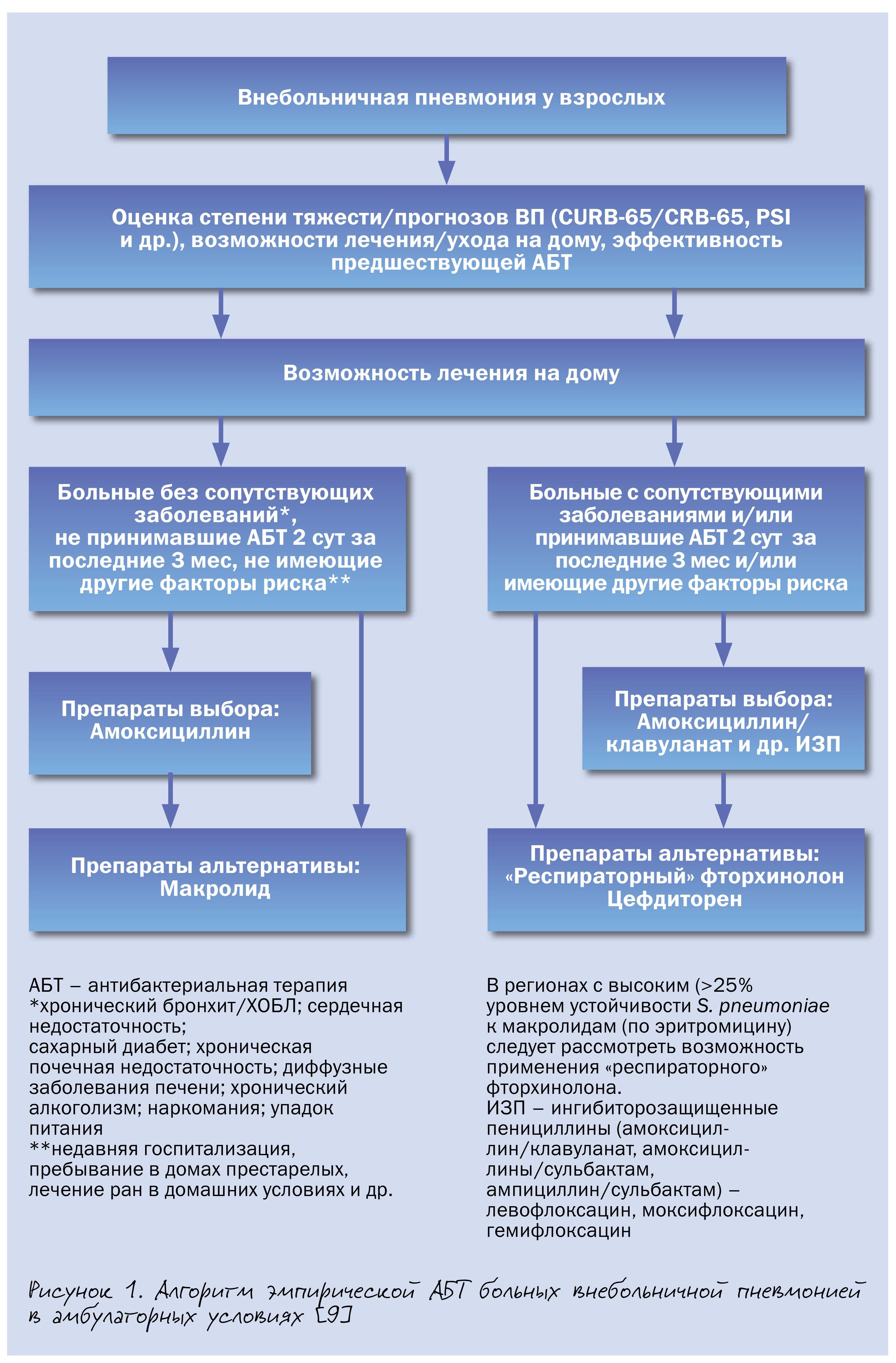
В данной клинической ситуации антибиотиком выбора является амоксициллин, альтернативы – макролиды. Последнее объясняется быстрым и существенным ростом устойчивости S. pneumoniae к макролидам в РФ и, как следствие этого, риском клинических неудач. Макролиды применяют, когда невозможно назначить амоксициллин (индивидуальная непереносимость, анамнестические указания на аллергические реакции немедленного типа на прием β-лактамов), а также при ВП микоплазменной или хламидийной этиологии.
Во вторую группу включены больные внебольничной пневмонией с сопутствующими заболеваниями (ХОБЛ, сахарный диабет, хроническая сердечная недостаточность, хроническая болезнь почек со снижением скорости клубочковой фильтрации, цирроз печени, алкоголизм, наркомания, истощение) и/или принимавшими за последние 3 мес. антибиотики в течение ≥2 последовательных дней и/или имеющими иные факторы риска инфицирования редкими и/или полирезистентными возбудителями. Поскольку вероятность этиологической роли грамотрицательных бактерий (в т. ч. обладающих некоторыми механизмами вторичной лекарственной устойчивости) у этих больных возрастает, то в качестве антибиотиков выбора рекомендуются ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.), а альтернативы – «респираторные» фторхинолоны и цефдиторен.
Подобный подход, предполагающий применение фторхинолонов в качестве альтернативной терапии, является общепринятым и обусловлен необходимостью уменьшить селекцию лекарственноустойчивых штаммов пневмотропных возбудителей и возможность их использования при неэффективности АБТ первого ряда. Несмотря на определенную роль «атипичных» возбудителей в этиологии внебольничной пенвмонии у пациентов данной группы, рутинное назначение комбинации β-лактамного антибиотика и макролида не рекомендуется, так как на сегодняшний день не доказано, что такая стратегия улучшает исходы лечения при возможном увеличении риска нежелательных лекарственных реакций и селекции антибиотикорезистентности.
При госпитализации пациента с внебольничной пневмонией прежде всего необходимо решить вопрос о месте лечения – отделение общего профиля или ОИТ. Крайне важно быстро выявить признаки тяжелой внебольничной пневмонии (табл. 2), так как данные пациенты требуют неотложной помощи в условиях ОИТ.
У госпитализированных пациентов возможно применение широкого круга АБТ – ампициллина, ингибиторозащищенных пенициллинов (амоксициллин/клавуланат и др.), цефалоспоринов с высокой антипневмококковой активностью (цефотаксим, цефтриаксон, цефтаролин), эртапенема, «респираторных» фторхинолонов, демонстрирующих в целом сопоставимую эффективность. Стратификация больных аналогична таковой для амбулаторных пациентов.Антибиотиками выбора у госпитализированных больных с нетяжелой ВП без сопутствующих заболеваний и других факторов риска инфицирования редкими и/или полирезистентными возбудителями является ампициллин, альтернативными – ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.) и «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин).
Антибиотиками выбора у госпитализированных больных с нетяжелой ВП при сопутствующих заболеваниях и других факторов риска инфицирования редкими и/или полирезистентными возбудителями будут ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.), цефалоспорины III поколения (цефотаксим, цефтриаксон), «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин), а у отдельных категорий пациентов – цефтаролин и эртапенем. Несмотря на различия в спектре активности in vitro эффективность указанных режимов АБТ у данной категории пациентов сопоставима.
В регионах с высокой распространенностью пенициллинорезистентных пневмококков (ПРП), при наличии индивидуальных факторов риска инфицирования ПРП определенные преимущества может иметь цефтаролин. У пожилых пациентов с множественной сопутствующей патологией и высоким риском неблагоприятного прогноза, наличии факторов риска аспирации, обитателей домов престарелых более эффективно назначение эртапенема.
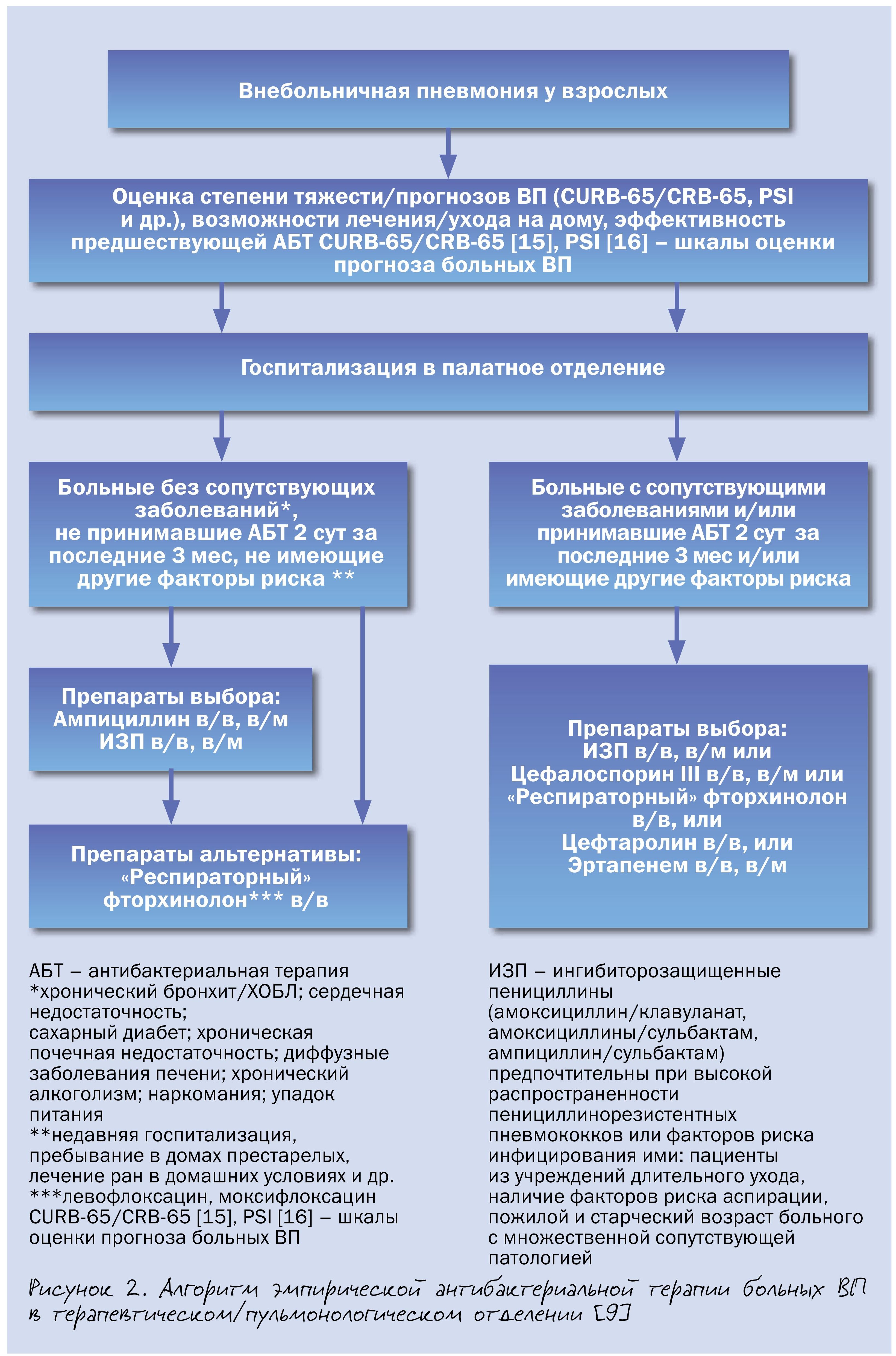
Имеющиеся доказательства превосходства комбинации «β-лактам + макролид» над монотерпией β-лактамами у госпитализированных больных ВП, полученные преимущественно в рамках обсервационных исследований, касаются, главным образом, тяжелого течения заболевания. Поэтому рутинное назначение комбинированной АБТ при нетяжелой ВП у госпитализированных пациентов нецелесообразно в связи с риском селекции антибиотикорезистентности (рис. 2).
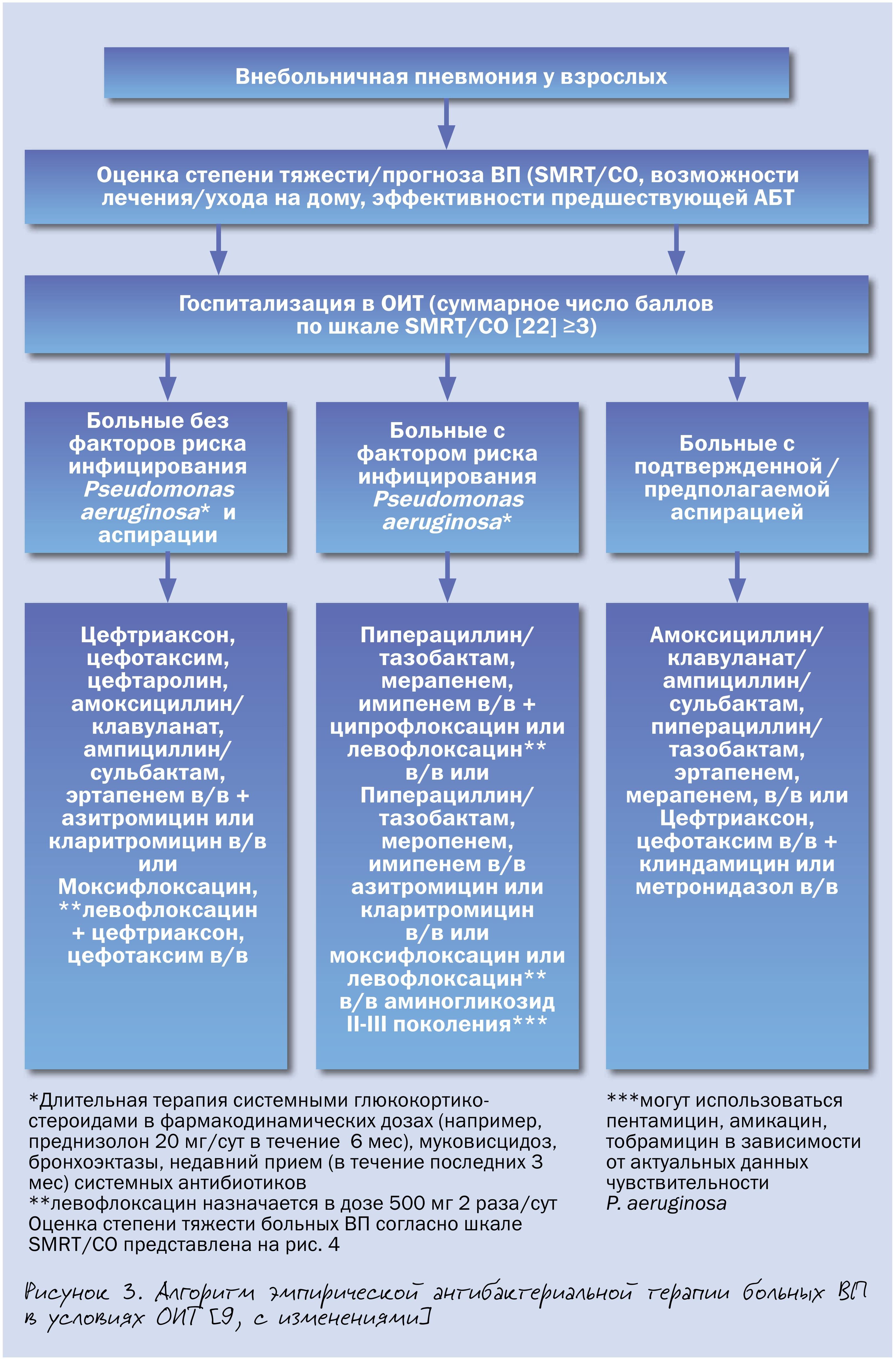
Алгоритм эмпирической антибиотикотерапии больных с тяжелым течением внебольничной пневмонией представлен на рис. 3, однако детальное обсуждение вопросов ведения данной категории пациентов не входило в задачи настоящей статьи.
Алгоритмизация как определенная последовательность врачебных действий, представляющихся оптимальными, может оказаться весьма полезной, особенно на начальном этапе ведения больного ВП, когда врач испытывает известный информационный дефицит (этиология заболевания? чувствительность возбудителя ВП к антибиотикам? возможные осложнения ВП? «ответ» пациента на введение первых доз антибиотика? и др.).

Доказательством этому являются, в частности, многочисленные свидетельства того, что следование клиническим рекомендациям, приближающим нас к диагностическому и лечебному универсализму, минимизирует стоимость лечения, сокращает сроки госпитализации и сопровождается снижением летальности. Вместе с тем доступность диагностических и терапевтических алгоритмов не освобождает нас от «индивидуального прочтения» актуальной клинической ситуации в отдельно взятой стране или регионе с учетом локальной антибиотикорезистентности, географической вариабельности этиологии внебольничной пневмонии, сложившихся лечебных традиций (но не укоренившихся заблуждений), и особенностей организации медицинской помощи на амбулаторном и госпитальном этапах. Иными словами, широкая популяризация клинических рекомендаций или их отдельных элементов (включая диагностические и лечебные алгоритмы) вовсе не означает утраты врачом разумной автономии.Источники:
Книги:
Нозокомиальная пневмония у взрослых. 2-е издание
Презентация:
Внебольничная пневмония
Внебольничная пневмония
Внебольничная пневмония
Пневмонии
14.01.2020 | 21:11:58
Источник
В апреле 2019 г. в Москве состоялись XXVI Российский национальный конгресс «Человек и лекарство» и III Саммит пульмонологов. В качестве ключевой темы Конгресса и Саммита были выбраны проблема внебольничной пневмонии, подходы к фармакотерапии в условиях растущей антибиотикорезистентности.
Внебольничная пневмония — острое заболевание, возникшее во внебольничных условиях, сопровождающееся симптомами инфекции нижних дыхательных путей (лихорадка, кашель, отделение мокроты, возможно гнойной, боль в груди, одышка) и рентгенологическими признаками «свежих» очагово-инфильтративных изменений в легких при отсутствии диагностической альтернативы.
Внебольничная пневмония является лидирующей причиной заболеваемости и смертности в мире и в Российской Федерации и представляет собой одну из самых частых причин госпитализации и смертности среди взрослых, особенно пожилых лиц.
Этиология внебольничной пневмонии
Глобально Streptococcus pneumoniae (S. pneumoniae) является основным возбудителем внебольничной пневмонии, вне зависимости от возраста и сопутствующей патологии. Однако в последнее время регистрируется все больше случаев пневмонии, вызванной респираторными вирусами. 50% всех вирусных причин внебольничной пневмонии приходятся на вирус гриппа, риновирусы и коронавирусы. Проблемы диагностики и терапии пациентов с вирусной внебольничной пневмонией стали темой для открытых дискуссий на Конгрессе «Человек и лекарство».
Полагают, что вирусная причина обуславливает 7–36% случаев внебольничной пневмонии [1, 2]. Так, по данным одного недавнего исследования, среди всех госпитализированных взрослых пациентов с внебольничной пневмонией у 9% был выявлен риновирус, у 6% — вирус гриппа и у 5% — S. pneumoniae [1]. В систематическом обзоре и метаанализе 2017 г. показано, что в европейских странах вирусы были диагностированы примерно у 22% пациентов, госпитализированных с рентгенологически подтвержденной внебольничной пневмонией [3].
Обращает на себя внимание, что вирусы чаще выявляют у пациентов с тяжелой пневмонией или осложненным течением заболевания (например, острым дистресс-синдромом) [4, 5]. К тому же выявляют сезонные вспышки вирусной пневмонии у маленьких детей и пожилых лиц, обусловленные вирусом гриппа и респираторно-синцитиальным вирусом [6]. В последние годы были зафиксированы случаи развития внебольничной пневмонии, вызванные метапневмовирусом, коронавирусом и бокавирусом (данные вирусы также ответственны за развитие тяжелой острой дыхательной недостаточности).
Помимо вирусной этиологии внебольничной пневмонии, настоящим вызовом для клиницистов становится ведение пациентов с мультирезистентной пневмококковой инфекцией.
Проблема резистентности возбудителей пневмонии к антибактериальным препаратам
В 2017 г. был опубликован систематический обзор, посвященный распространенности, механизмам развития и клиническим последствиям резистентности S. pneumoniae к антибиотикам [7]. Отмечено, что резистентность к пенициллинам обусловлена генетическими структурными изменениями в пенициллин-связывающих белках. Резистентность к макролидам варьирует от 20% до 40%. Основными механизмами резистентности выступают изменение рибосомальной мишени действия, изменение транспорта антибиотика и модификация самого антибиотика. Примерно 22% изолятов S. pneumoniae были резистентны к клиндамицину, основным механизмом нечувствительности являлось изменение мишени действия. Показано, что резистентность к фторхинолонам низка, однако наблюдается тенденция к повышению ее частоты. Основными механизмами резистентности выступают накопление мутаций в бактериальном геноме, повышение выведения антибиотика из бактериальных клеток или приобретение плазмид-кодирующих генов. Также показан рост резистентности пневмококка к тетрациклинам. Резистентность обусловлена двумя генами, обеспечивающими защиту рибосом.
Обращает на себя внимание растущая резистентность S. pneumoniae к макролидам. Резистентность к макролидам, как было сказано выше, обусловлена несколькими механизмами. В Северной Америке наиболее частым механизмом является активное выведение антибиотиков из бактериальных клеток, что обеспечивает низкий уровень устойчивости к макролидам. В Европе самым частым механизмом выступают изменение мишени действия (метилирование рибосом), что ассоциировано с высоким уровнем резистентности. Обращает на себя внимание, что в России резистентность может быть обусловлена и тем, и другим механизмом. а также мутациями в 23S рРНК и рибосомальных белках L4.
В 2018 г. были представлены результаты исследования чувствительности изолятов S. pneumoniae (n = 279) и Haemophilus influenzae (H. influenzae) (n = 279), собранных в России в 2014–2016 гг. [8]. Показано, что чувствительность к оральным пенициллинам и макролидам была низкой у S. pneumoniae. При этом чувствительность была 100% к фторхинолонам и ≥ 92,8% к амоксициллину, амоксициллину/клавуланату и цефтриаксону. Изоляты H. influenzae имели сниженную чувствительность к ампициллину, цефаклору и кларитромицину.
Таким образом, отмечается рост резистентности пневмококка к различным антибактериальным препаратам, что диктует необходимость поиска новых эффективных молекул и рациональное использование имеющихся антибиотиков.
Факторы риска антибиотикорезистентных возбудителей внебольничной пневмонии
Факторами риска внебольничной пневмонии, вызванной грамотрицательными бактериями, включая Pseudomonas, являются ранее проводимая антибактериальная терапия, недавние госпитализации, иммуносупрессивная терапия, легочные коморбидные состояния (например, легочный фиброз, бронхоэктазы, частые обострения хронической обструктивной болезни легких (ХОБЛ), требующие назначения глюкокортикоидов и/или антибиотиков), потенциальная аспирация, наличие коморбидных заболеваний (например, алкоголизм, сахарный диабет). Результаты международного проспективного исследования, включавшего 3193 пациента, госпитализированных с внебольничной пневмонией, показали, что Pseudomonas aeruginosa (P. aeruginosa) встречалась у 4,2% пациентов. При этом изоляты Pseudomonas имели лекарственную резистентность практически в половине случаев. Были выявлены независимые факторы риска инфекции P. aeruginosa. Они включали указание в анамнезе на инфекцию/колонизацию Pseudomonas (отношение шансов (ОШ) 16), трахеостомию (ОШ 6), бронхоэктазы (ОШ 3), необходимость в респираторной и вазопрессивной поддержке (ОШ 2) и очень тяжелую ХОБЛ (ОШ 3) [9].
Факторами риска пневмонии, вызванной метициллин-резистентным Staphylococcus aureus, считаются поздняя стадия почечной недостаточности, контактный вид спорта, использование инъекционных наркотиков, скученное проживание, половые контакты мужчин с мужчинами, недавний грипп в анамнезе, антимикробная терапия (особенно фторхинолоны) в последние 3 месяца, некротическая или казеозная пневмония, наличие эмпиемы.
Факторами риска лекарственно-устойчивой пневмонии, вызванной S. pneumoniae являются возраст > 65 лет, применение бета-лактамных антибиотиков, макролидов или фторхинолонов в последние 3–6 месяцев, алкоголизм, коморбидность, иммуносупрессивные состояния или терапия. Обращает на себя внимание, что недавняя терапия или повторные курсы бета-лактамов, макролидов и фторхинолонов являются фактором риска резистентности пневмококка к тем же самым классам антибиотиков [9]. Именно поэтому таким пациентам необходимо назначать альтернативные антибактериальные препараты.
Спорные аспекты диагностики внебольничной пневмонии
Диагностика внебольничной пневмонии основана на клинической картине заболевания (наличие кашля, мокроты, боли в грудной клетке, повышения температуры тела) и данных рентгенологического исследования обычно, радиографии (рентгенографии) органов грудной клетки. В настоящее время альтернативой радиографии (рентгенографии) считается ультразвуковое исследование (УЗИ) легких. По данным метаанализа 2017 г., включавшего 12 исследований (1515 взрослых пациентов), чувствительность УЗИ в диагностике пневмонии составила 88%, специфичность 86% [10].
Непосредственное обследование больного является важным компонентом диагностики, однако менее специфично и чувствительно, чем радиографическое исследование. Обращает на себя внимание, что симптомы и результаты физикального обследования могут отсутствовать или быть изменены у пожилых пациентов. Всем пациентам также следует выполнить пульсоксиметрию для диагностики гипоксемии.
В рамках Конгресса «Человек и лекарство» прошла школа для практикующих врачей по пульмонологии, в рамках которой в интерактивном формате обсуждалась лабораторная диагностика пневмонии.
Микробиологическое исследование позволяет выявить возбудителя пневмонии, однако рутинные тесты часто дают ложноотрицательный результат. В международных рекомендациях, включая рекомендации Американского инфекционного общества и Американского торакального общества, говорится о необходимости поиска антигена в моче к S. pneumoniae и Legionella pneumophila (L. pneumophila) у пациентов с внебольничной пневмонией. Однако результаты недавнего исследования свидетельствуют, что из 1941 пациента, включенного в анализ, только у 4% был позитивный тест на S. pneumoniae и у 2% пациентов положительный тест на L. pneumophila. По данным мультивариантного анализа не было выявлено предикторов положительного теста на S. pneumoniae. Для L. pneumophila гипонатриемия, лихорадка и диарея были достоверно ассоциированы с положительным тестом на антиген [11].
Одним из лабораторных тестов, который вызывает дискуссию у клиницистов, является воспалительный маркер прокальцитонин. Сторонники определения прокальцитонина приводят аргументы в пользу более рационального назначения антибиотикотерапии. Результаты систематического обзора 14 рандомизированных клинических исследований говорят, что использование высокочувствительного показателя прокальцитонина ассоциировано со снижением частоты назначения антибиотиков и сокращением длительности терапии [12].
Однако результаты некоторых клинических исследований оспаривают данный факт. Так, по данным рандомизированного контролируемого исследования показано, что антибиотикотерапия, назначаемая на основании уровня прокальцитонина, не ассоциирована со снижением дней применения антибиотика и более низкой частотой неблагоприятных исходов [13].
Другим маркером воспаления, который рекомендуется определять при внебольничной пневмонии, является С-реактивный белок. Показано, что наибольшую ценность с практической точки зрения данный маркер представляет при неопределенном диагнозе (отсутствие четкой рентгенологической картины у пациентов с характерным анамнезом, жалобами и данными непосредственного обследования, свидетельствующими в пользу легочной консолидации). Если концентрация С-реактивного белка ≥ 100 мг/л — его специфичность в подтверждении диагноза превышает 90%, если же показатель не превышает 20 мг/л — диагноз внебольничной пневмонии является маловероятным [14].
Антибактериальная терапия внебольничной пневмонии
На Конгрессе «Человек и лекарство» и III Саммите пульмонологов детально обсуждались принципы рациональной антибактериальной терапии у больных пневмонией. Важно подчеркнуть, что при выборе терапии следует ориентироваться на данные о локальной резистентности, наличие сопутствующих заболеваний, указание в анамнезе на аллергические реакции, а также наличие антибиотикотерапии в течение 3 предшествующих месяцев.
В качестве терапии нетяжелой внебольничной пневмонии, проводимой амбулаторно, у пациентов без сопутствующих заболеваний, не принимавших в течение последних 3 месяцев антибиотиков, следует выбрать амоксициллин, его альтернативой считается макролид (азитромицин, кларитромицин). Если же речь идет о пациентах с сопутствующими заболеваниями и/или указанием в анамнезе на антибиотикотерапию на протяжении последних 3 месяцев, препаратом выбора является амоксициллин/клавуланат, альтернативным препаратом — респираторный фторхинолон или цефалоспорин 3-го поколения [15].
Клиницистам следует помнить, что в регионах с высоким (> 25%) уровнем устойчивости S. pneumoniae к макролидам следует рассмотреть возможность применения респираторного хинолона; при известной или предполагаемой микоплазменной этиологии в районах с высоким (> 25%) уровнем устойчивости M. pneumoniae к макролидам следует рассмотреть возможность применения респираторного хинолона или доксициклина.
Парентеральные антибиотики при лечении пневмонии в амбулаторных условиях не имеют доказанных преимуществ перед пероральными, при этом ассоциированы с повышением частоты постинъекционных осложнений и более высокими затратами на введение [15].
При лечении нетяжелой внебольничной пневмонии в стационаре у пациентов без сопутствующих заболеваний и не получавших антибиотики на протяжении 3 последних месяцев предпочтение следует отдать амоксициллину/клавуланату в/в, в/м или ампициллину в/в, в/м, альтернативой служит левофлоксацин или моксифлоксацин в/в. У пациентов с нетяжелой пневмонией с сопутствующими заболеваниями и/или принимавшими за последние 3 месяца антимикробные препараты, следует выбирать между амоксициллином/клавуланатом в/в, в/м, или цефалоспорином 3-го поколения (цефотаксим, цефтриаксон) в/в, в/м, или респираторным фторхинолоном (левофлоксацин, моксифлоксацин) в/в, или эртапенемом в/в, в/м [15].
Какова же оптимальная продолжительность антибактериальной терапии при внебольничной пневмонии? Четкого ответа на этот вопрос не получено. Считается, что длительность терапии зависит от возраста, сопутствующих заболеваний, наличия осложнений и др. Решение о прекращении терапии должно основываться на клинических данных (стойкое снижение температуры тела ≤ 37,2 °C в течение не менее 48 ч; отсутствие интоксикационного синдрома; частота дыхания < 20 в 1 мин (у пациентов без хронической дыхательной недостаточности); отсутствие гнойной мокроты (за исключением пациентов с ее постоянной продукцией), тогда как рентгенологическая картина отстает по времени от клинических показателей. При таком подходе длительность применения антибиотиков у большинства пациентов не превышает 7–10 дней [14].
В настоящее время активно обсуждаются способы профилактики внебольничной пневмонии. Наибольшую доказательную силу имеет вакцинация против гриппа у всех пациентов и против пневмококка у пациентов 65 лет и старше и лиц из высокой группы риска. Слушатели Конгресса «Человек и лекарство» приняли участие в апробации клинического алгоритма ведения пациентов на этапе оказания первичной медико-санитарной помощи по вакцинопрофилактике.
Говоря о профилактике пневмонии, нельзя не упомянуть меры по изменению образа жизни, и в первую очередь отказ от курения. Результаты недавних исследований свидетельствуют, что курение повышает предрасположенность к бактериальным легочным инфекциям, в том числе и у пассивных курильщиков. Следует отметить, что связь между курением и риском пневмонии носит дозозависимый эффект, при этом риск снижается через 10 лет после прекращения курения до такового у некурящих индивидуумов. Важно отметить, что прогноз пневмококковой пневмонии хуже у курильщиков.
Заключение
Диагностика и лечение внебольничной пневмонии стали сюжетом для научного обсуждения на национальном Конгрессе «Человек и лекарство» и III Саммите пульмонологов. Подходы к рациональной фармакотерапии заболевания были обсуждены в свете российских данных по антибиотикорезистентности. В профилактике внебольничной пневмонии важная роль отводится вакцинации против пневмококка и гриппа. В рамках Конгресса «Человек и лекарство» и III Саммита пульмонологов проходила апробация клинических алгоритмов ведения пациентов на этапе оказания первичной медико-санитарной помощи с частыми встречающимися общеврачебными нозологиями, в том числе алгоритма по вакцинопрофилактике.
Литература
- Jain S., Self W. H., Wunderink R. G. et al. Community-Acquired Pneumonia Requiring Hospitalization // N Engl J. Med. 2015; 373: 2382.
- Wu X., Wang Q., Wang M. S. et al. Incidence of respiratory viral infections detected by PCR and real-time PCR in adult patients with community-acquired pneumonia: a meta-analysis // Respiration. 2015; 89: 343–352.
- Alimi Y., Lim W. S., Lansbury L. et al. Systematic review of respiratory viral pathogens identified in adults with community-acquired pneumonia in Europe // J Clin Virol. 2017; 95: 26–35.
- Piralla A., Rovida F., Girello A. et al. Frequency of respiratory virus infections and next-generation analysis of influenza A/H1N1pdm09 dynamics in the lower respiratory tract of patients admitted to the ICU // PloS One. 2017; 12: e0178926.
- Shah R. D., Wunderink R. G. Viral Pneumonia and Acute Respiratory Distress Syndrome // Clin Chest Med. 2017; 38: 113–125.
- Scheltema N. M., Gentile A., Lucion F. et al. Global respiratory syncytial virus-associated mortality in young children (RSV GOLD): a retrospective case series // Lancet Glob Health. 2017; 5: e984–991.
- Cherazard R., Epstein M., Doan T. L. et al. Antimicrobial Resistant Streptococcus pneumoniae: Prevalence, Mechanisms, and Clinical Implications // Am J Ther. 2017; 24 (3): e361–e369.
- Torumkuney D., Mayanskiy N., Edelstein M. et al. Results from the Survey of Antibiotic Resistance (SOAR) 2014–16 in Russia // J Antimicrob Chemother. 2018; 73 (suppl. 5): v. 14–21.
- Restrepo M. I., Babu B. L., Reyes L. F. et al. Burden and risk factors for Pseudomonas aeruginosa community-acquired pneumonia: a multinational point prevalence study of hospitalised patients // Eur Respir J. 2018; 52.
- Long L., Zhao H. T., Zhang Z. Y. et al. Lung ultrasound for the diagnosis of pneumonia in adults: A meta-analysis // Medicine (Baltimore). 2017; 96 (3): e5713.
- Bellew S., Grijalva C. G., Williams D. J. et al. Pneumococcal and Legionella Urinary Antigen Tests in Community-acquired Pneumonia: Prospective Evaluation of Indications for Testing // Clinical Infectious Diseases. 2019; 68 (12): 2026–2033.
- Schuetz P., Chiappa V., Briel M., Greenwald J. L. Procalcitonin algorithms for antibiotic therapy decisions: a systematic review of randomized controlled trials and recommendations for clinical algorithms // Arch Intern Med. 2011; 171(15): 1322–1331.
- Huang D. T., Yealy D. M., Filbin M. R. et al. Procalcitonin-Guided Use of Antibiotics for Lower Respiratory Tract Infection // N Engl J Med. 2018; 379: 236–249.
- Рачина С. А., Синопальников А. И. Клинические рекомендации по внебольничной пневмонии у взрослых: что нас ждет в 2019 г // Практическая пульмонология. 2018; 3: 8–13.
- Федеральные клинические рекомендации. Внебольничная пневмония. 2018.
Ю. В. Евсютина, кандидат медицинских наук
ФГБУ НМИЦПМ Минздрава России, Москва
Контактная информация: evsyutina.yulia@gmail.com
DOI: 10.26295/OS.2019.89.41.013
Внебольничная пневмония, коротко о главном. Что важно знать практикующему врачу. По материалам Конгресса «Человек и лекарство» и III Саммита пульмонологов/ Ю. В. Евсютина
Для цитирования: Лечащий врач № 11/2019; Номера страниц в выпуске: 56-59
Теги: дыхательные пути, инфекции, профилактика, вакцинация
Купить номер с этой статьей в pdf
Источник


