Этиопатогенетическая терапия острых средних отитов
Методические рекомендации. Утверждены Главным оториноларингологом Минздрава России Ю.К. Яновым 03 июля 2003 г. Санкт-Петербург. 2003.
Составители: зам. директора Санкт-Петербургского НИИ уха, горла, носа и речи, профессор С.В. Рязанцев.
Методические рекомендации одобрены Правлением Российского общества оториноларингологов.
Актуальность проблемы. Острый отит является одной из наиболее частых острых воспалительных инфекций у взрослых, еще чаще он встречается у детей. До 95% детей переносят хотя бы один эпизод острого среднего отита за первые 7 лет жизни.
Острый средний отит (ОСО) – остро развившееся воспаление полостей среднего уха с характерными симптомами (боль в ухе, повышение температуры, выделения из уха, снижение слуха, у детей – возбуждение, раздражительность, рвота, понос);
Затянувшийся острый средний отит (ЗОСО) – наличие симптомов воспаления среднего уха в течение 3-12 месяцев после одного или двух курсов антибиотикотерапии;
Рецидивирующий острый средний отит (РОСО) – наличие трех и более эпизодов ОСО за период 6 месяцев или 4 и более эпизодов за период 12 месяцев.
Стадии клинического течения острых средних отитов: I. Острый евстахеит. II. Острое (доперфоративное) катаральное воспаление. III. Острое гнойное воспаление (появление перфорации). IV. Постперфоративная стадия. V. Репаративная стадия.
Лечение острых средних отитов.
Стадия евстахеита. Эуфорбиум композитум Назентропфен С интраназально для снижения повышенной нагрузки на среднее ухо;
Стадия острого гнойного доперфоративного воспаления:
— осмотически активные местные препараты: спиртовые растворы борной кислоты, нитрофурала (фурациллина), левомицетина;
— анальгезирующая терапия: капли Отипакс, капли Анауран. Траумель С перорально капли, таблетки, мазь Траумель С на турунде в наружный слуховой проход, втирание мази в область сосцевидного отростка. Вибуркол свечи для ректального введения пациентам с болевым синдромом на фоне стойкого субфебрилитета.
— разгрузочная терапия: сосудосуживающие препараты (деконгексанты) в виде носовых капель — эфедрина гидрохлорид, ксилометазолин тетразолин, перорально псевдоэфедрин, фенилпропаноламин в комбинации с антигистаминными препаратами. Применение местно не более 5-7 дней из-за опасности угрозы передозировки и развития синдрома «рикошета» — медикаментозного ринита. Безопасно применение спрея Эуфорбиум композитум Назентропфен С в качестве дозированного аэрозоля. Усиливают эффект препрарата Эуфорбиум композитум Назентропфен С капли Лимфомиозот (лимфодренажное средство) и Эскулюс композитум (венотонизирующий препарат);
— противовоспалительная терапия: нестероидные противовоспалительные средства — ибупрофен, диклофенак; слабые ингибиторы синтеза простагландинов — индометацин, пироксикам; блокатор Н1-рецепторов, антагонист медиаторов воспаления — фенспирид; лекарственные формы средства с выраженным противовоспалительным и анальгезирующим эффектом Траумель С для местного и общего применения.
— системная антибиотикотерапия: Амоксициллин, Флемоксин-Солютаб (растворимые таблетки амоксициллина), Ко-амоксиклав (амоксициллин+ клавулоновая кислота), цефалоспорины (Цефуроксим аксетил); не назначать тетрациклин, линкомицин, гентамицин, ко-тримоксазол, аминогликозиды (токсическое поражение нейросенсорных клеток!).
Безопасен «биологический антибиотик» Эхинацея композитум СН.
— секретолитическая терапия: синупрет, Мукоза композитум – многокомпонентное средство для восстановления слизистых оболочек. Комплексные катализаторы обменных процессов Коэнзим композитум и Убихинон композитум.
Постперфоративная стадия острого среднего отита. Отказ от анальгезирующей терапии, исключение осмотически активных препаратов на спиртосодержащей основе. Полное исключение средств, содержащих аминогликозидные антибиотики: софрадекс, гаразон, полидекс, анауран. Разрешаются неототоксичные антибиотики: рифамицин – ушные капли отофа, ципрофлоксацин – ушные капли ципромед.
Показаны биологические комплексные ампулированные препараты: Траумель С, Эхинацея композитум СН, Мукоза композитум, Коэнзим композитум, Убихинон композитум, спрей Эуфорбиум композитум Назентропфен С.
Стадия репарации: Контроль рубцевания краев перфорации: прижигание 40% раствором йода и ляписа. Лазеротерапия. Самостоятельные курсы восстановительной терапии препаратами Траумель С, Плацента композитум.
Источник
Комментарии
Опубликовано в журнале:
«Эффективная фармакотерапия. Пульмонология и оториноларингология», 2012, № 3, с. 8-13
К.м.н. М.А. Панякина, д.м.н. А.Ю. Овчинников
МГМСУ, кафедра оториноларингологии факультета постдипломного образования
В работе проведена оценка эффективности Биопарокса и Эреспала в составе комплексной терапии острого тубоотита на фоне ОРВИ и ее сравнение с традиционным способом лечения топическими деконгестантами. Отмечена возможность достижения выздоровления в более короткие сроки лечения, а также уменьшения дозы деконгестантов при проведении комплексной патогенетической терапии тубоотита.
Патология среднего уха является актуальной проблемой современной оториноларингологии. Воспалительные и невоспалительные заболевания среднего уха нередко приводят к тяжелым, угрожающим жизни осложнениям и часто являются причиной потери слуха [1, 2]. Одним из ведущих этиопатогенетических факторов, приводящих к патологии среднего уха, и в частности кондуктивной тугоухости, является дисфункция слуховой трубы [3, 4].
Среди большого разнообразия причин развития тубоотитов важное место отводится патологии полости носа и околоносовых пазух [5, 6], в большинстве случаев дебютирующей на фоне ОРВИ [7].
Вирусная природа данных состояний не требует назначения антибактериальной терапии, однако в ряде случаев в патологический процесс вовлекается сапрофитная микробная флора и возникают бактериальные осложнения со стороны как верхних (отит, лимфаденит, тонзиллит, фарингит и др.), так и нижних отделов (бронхит, пневмония, трахеобронхит и др.) дыхательных путей [8].
Очевидно, что появление признаков бактериального осложнения является абсолютным показанием к назначению противомикробной терапии. В этом смысле широкое использование антибактериальных препаратов с целью предупреждения присоединения микробной инфекции вполне понятно. Однако такая терапия нередко приводит к нежелательным последствиям — развитию дисбиоза, аллергизации организма и др., а также влечет за собой проблему развития антибиотикорезистентности [9]. Поскольку с практической точки зрения избежать применения антибактериальных средств при бактериальных осложнениях ОРВИ не представляется возможным, остро встает вопрос о минимизации нежелательных последствий системных антибактериальных средств. В этой связи особый интерес представляют антибиотики местного применения. Очевидно, что при таком способе введения больше оснований рассчитывать на высокую эффективность, поскольку создается нужная концентрация антибактериальных средств непосредственно в зоне поражения и одновременно удается избежать системного их действия [8]. Согласно данным литературы, наиболее полно этим требованиям отвечает аэрозольный препарат Биопарокс, представляющий собой антибиотик фузафунгин для местного применения [10]. Показано, что после ингаляционного применения препарата Биопарокс фузафунгин не определяется в плазме крови, а остается на поверхности слизистой оболочки дыхательных путей [11].
Помимо местной антибактериальной терапии в случаях развития тубоотита на фоне острого назофарингита в рамках ОРВИ абсолютно показано проведение так называемой разгрузочной терапии, направленной на уменьшение отека слизистой оболочки полости носа и устьев слуховых труб. Реализация данного направления может осуществляться различными способами. Чаще всего с этой целью применяют топические деконгестанты, преимуществом которых, в первую очередь, является быстрота достижения необходимого эффекта. Но ограничение длительности приема данных препаратов 7 днями, а также существенные побочные эффекты — факторы, которые в ряде случаев не позволяют однозначно сделать выбор в пользу данной группы препаратов.
С разгрузочной целью могут применяться и антигистаминные средства, которые, однако, более показаны при сопутствующих аллергических заболеваниях, в то время как в отсутствие таковых их применение может быть не столь эффективным. Эффективность интраназальных кортикостероидов с целью уменьшения отека и повышенной экссудации слизистой оболочки полости носа была доказана в огромном количестве исследований, поскольку данные препараты, несомненно, характеризуются рядом существенных преимуществ, связанных прежде всего с возможностью длительного применения, минимальным количеством побочных эффектов и сравнительно быстрым наступлением эффекта [12]. Согласно мнению ряда авторов, их применение во время ОРВИ абсолютно обосновано с целью профилактики развития застойных явлений, связанных с противовоспалительным действием. Тем не менее данные, свидетельствующие о том, что применение топических стероидов в течение вирусной фазы воспалительного процесса негативно влияет на состояние местного иммунитета, диктуют применение более дифференцированного подхода при острой вирусной фазе респираторного заболевания. Однако воспалительный процесс бактериальной этиологии не является противопоказанием для назначения современных топических кортикостероидов [13]. Для разгрузочной терапии могут применяться также препараты, которые могут найти множество точек приложения при лечении состояний с «неоднозначной» этиологией. В этой связи наше внимание привлек препарат Эреспал (фенспирид), действие которого направлено на различные звенья воспалительного процесса: образование производных арахидоновой кислоты, синтез и выброс гистамина и цитокинов. Этот факт резко выделяет его из общего ряда противовоспалительных, стероидных и нестероидных препаратов, оказывающих влияние преимущественно на уровне метаболизма арахидоновой кислоты [14]. Учитывая вышеизложенное, проведено исследование, целью которого была оптимизация лечения больных острым тубоотитом.
Материал и методы исследования
Под наблюдением находилось 64 пациента (38 женщин и 26 мужчин) в возрасте от 20 до 65 лет (средний возраст 42,3 ± 5,1 года) с диагнозом «острый тубоотит», подтвержденным клинико-анамнестическими данными и результатами лабораторно-инструментальных методов исследования. У всех пациентов заболевание развилось на фоне острого назофарингита в рамках ОРВИ, по поводу которого лечебные мероприятия не проводились, а поводом обращения к врачу послужили симптомы со стороны органа слуха (табл.). Длительность от момента заболевания ОРВИ до появления симптомов тубоотита варьировала от 1 суток до 3 дней (1,4 ± 1,2 дня).
Таблица. Клиническая характеристика исследуемых пациентов
| Параметр | Основная группа | Контрольная группа | Р |
| Количество больных, чел. | 33 | 31 | нд* |
| Женщины, чел. | 19 | 19 | нд |
| Мужчины, чел. | 14 | 12 | нд |
| Возраст, лет | 35,2 ± 7,1 | 34,8 ± 5,4 | нд |
Клинические данные | |||
| Основные жалобы | Заложенность уха, снижение слуха, шум в ухе | Те же | – |
| Слух (шепотная речь), м | 2,5 ± 0,4 | 2,7 ±0,6 | нд |
| Аудиометрия (тип тугоухости, КВИ), дБ | Кондуктивная тугоухость с КВИ 27,6 ± 0,5 на речевых частотах | Кондуктивная тугоухость с КВИ 28,9 ± 0,8 на речевых частотах | нд |
| Тимпанометрия, даПа | Тип С (90,1%) — смещение тимпанометрической кривой влево (от -50 до -300 и ниже) | Тип С (90,3%) — смещение тимпанометрической кривой влево (от -50 до -300 и ниже) | нд |
| Проходимость слуховых труб | Выраженное нарушение проходимости слуховой трубы (3-5-й степени) в 84,8% | Выраженное нарушение проходимости слуховой трубы (3-5-й степени) в 80,6% | нд |
КВИ — костно-воздушный интервал.
* нд — различия статистически недостоверны.
В исследование не включались пациенты, имевшие в анамнезе аллергические заболевания, в том числе аллергический ринит, а также нуждавшиеся в одновременном назначении других системных антимикробных препаратов в связи с сопутствующей патологией, поскольку правильная интерпретация результатов исследования в данных случаях могла быть существенно затруднена. Диагноз заболевания устанавливался на основании типичных клинических симптомов и данных аудио- и тимпанометрии. В зависимости от тактики лечения больные были рандомизированы на 2 группы — основную (ОГ) и контрольную (КГ), различия по возрасту и полу, а также основным клиническим характеристикам заболевания между которыми были статистически недостоверными (табл.). В основной группе схема лечения предусматривала назначение фузафунгина (препарат Биопарокс) в дозировке 2 ингаляции препарата в каждый носовой ход 4 раза в сутки, при необходимости в комбинации с 4 ингаляциями препарата 4 раза в сутки перорально в течение 7 дней; фенспирида (препарат Эреспал) в дозировке 80 мг 2-3 раза в сутки в течение 7 дней, а также ирригационной терапии интраназально и топических деконгестантов. В контрольной группе применялась ирригация полости носа в сочетании с деконгестантами в течение 7 дней. Поскольку заболевание дебютировало в течение острой фазы вирусной инфекции, такие традиционные методы лечения тубоотита, как продувание ушей по Политцеру и пневмомассаж барабанных перепонок, не проводились по причине высокой вероятности попадания патогенной микрофлоры в другие отделы среднего уха. Длительность наблюдения составила 7 дней.
Эффективность проводимого лечения оценивалась при входном обследовании и на 7-е сутки от начала лечения и определялась по степени уменьшения субъективных и объективных симптомов тубоотита по трехбалльной системе до и после лечения. Выделяли следующие параметры оценки:
- отсутствие эффекта: сохранение субъективных и объективных признаков тубоотита после лечения;
- улучшение: существенное уменьшение субъективных и/или объективных признаков тубоотита после лечения;
- выздоровление: полное исчезновение субъективных и объективных симптомов тубоотита после лечения.
Результаты исследования и их обсуждение
Согласно полученным результатам, в ОГ выраженность субъективных ощущений тубоотита, а также объективные симптомы достоверно уменьшались к 7-м суткам терапии. При этом отмечены статистически достоверные различия по исследуемым параметрам при сравнении таковых в контрольной группе. Так, к 7-и суткам лечения результаты тимпанометрии свидетельствовали о нормализации давления в барабанных полостях у пациентов ОГ, в то время как в КГ данный показатель к концу лечения сохранялся отрицательным (р Рис. 1. Динамика данных тимпанометрии у исследуемых пациентов
Аналогичной была динамика результатов аудиометрии: среднее значение костно-воздушного интервала у пациентов ОГ к концу лечения было достоверно меньшим по сравнению с показателем в КГ (р Рис. 2. Динамика данных аудиометрии у исследуемых пациентов
Рис. 3. Динамика проходимости слуховых труб у исследуемых пациентов
Рис. 4. Сравнительная эффективность проведенного лечения
Таким образом, результаты проведенного исследования подтверждают высокую эффективность и безопасность комплексной терапии с включением фузафунгина (препарат Биопарокс), фенспирида (препарат Эреспал), топических деконгестантов и средств для ирригации полости носа у больных с острым тубоотитом на фоне ОРВИ, что выражалось в более быстрой динамике исчезновения субъективных и объективных клинических симптомов. Эта тактика лечения позволяет существенно сократить долю использования топических деконгестантов, уменьшая вероятность развития побочных эффектов, свойственных данной группе лекарственных средств.
ЛИТЕРАТУРА
1. Жук Р.В. Секреторный средний отит: патофизиология и результаты лечения в разных возрастных группах // Вестник оториноларингологии: Материалы III Всероссийской научно-практической конференции «Наука и практика в оториноларингологии». М., 2004. С. 188-190.
2. Рязанцев С.В. Этиопатогенетическая терапия острых средних отитов: методические рекомендации. СПб., 2003. 26 с.
3. Бобошко М.Ю. Вопросы патогенеза, диагностики и лечения дисфункций слуховой трубы: Дисс. … докт. мед. наук. СПб., 2005. 242 с.
4. Крюков А.И., Туровский А.Б., Шубин М.Н. Результаты эндоскопического исследования у больных с длительной тубарной дисфункцией // Вестник оториноларингологии. 2002. № 6. С. 6-8.
5. Янов Ю.Ж., Рязанцев СВ. Этиопатогенетическая терапия острых средних отитов // Consilium medicum. 2005. Т. 7. № 4. С. 290-297.
6. Lim D.J., Chun Y.M., Lee H.Y. et al. Cell biology of tubotympanum in relation to pathogenesis of otitis media — a review // Vaccine. 2000. Vol. 19. Suppl. 1. P. S17-S25.
7. Heikkinen Т., Chonmaitree T. Increasing importance of viruses in acute otitis media // Ann. Med. 2000. Vol. 32. № 3. P. 157-163.
8. Кладова О.В., Харламова Ф.С, ФельдфиксЛ.И. и др. Эффективность и безопасность лечения Биопароксом острых респираторных заболеваний с бактериальными осложнениями // Инфекции и антимикробная терапия. 2006. Т. 8. № 2. С. 22-24.
9. Таточенко В.Ж. Практическая пульмонология детского возраста. М., 2001. 268 с.
10. Adam D. Eroffnug der Arbeitstagund der Sektion Antimikrobielbe Chemotherapie der Paul-Ehrlich-gesellschaft 1985, Munchen // FAC Fortschr. Antimikr. Antineoplast. Chemother. 1987. Vol. 6-1.
11. Newman S.P, Steed K.R, Hooper G. et al. Scintigraphic assessment of the oropharyngeal and nasal depositions of fusafungine from a pressurized inhaler and from a novel pump spray device // J. Pharm. Pharmacol. 1995. Vol. 47. № 10. P. 818-821.
12. Fokkens W, Lund V., Mullol ].; European Position Paper on Rhinosinus-itis and Nasal Polyps group. European position paper on rhino sinusitis and nasal polyps 2007 // Rhinol. Suppl. 2007. № 20. P. 1-136.
13. Wallace D.V., Dykewicz M.S., Bernstein D.I. et al. The diagnosis and management of rhinitis: an updated practice parameter // J. Allergy Clin. Immunol. 2008. Vol. 122. № 2. Suppl. P. S1-S84.
14. Половщиков А.В. Фенспирид (Эреспал) — рациональные направления использования // Клиническая фармакология и терапия. 2002. № 5. С. 37-40.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
В статье представлены результаты исследования, посвященного оценке сравнительной эффективности, переносимости и безопасности применения лекарственных препаратов, содержащих феназон и лидокаин, в местной терапии острого среднего отита у детей.
Среди пациентов оториноларингологического профиля острый средний отит (ОСО) диагностируется в 20–30% случаев. Особенно часто это заболевание развивается у детей. Наиболее высокие показатели распространенности наблюдаются среди пациентов возрастной группы от 1 года до 4 лет (61,0%) и в течение первого года жизни (45,3%). Среди пациентов 35–44 лет распространенность ОСО составляет 1,5%, старше 75 лет — 2,3% [1–3]. Среди дошкольников распространенность ОСО составляет 80–90%, у 40% из них число эпизодов ОСО доходит до 6 в год [4–5]. В 2017 г. в Бразилии было проведено проспективное когортное исследование среди детей от 6 мес. до 5 лет. По его результатам заболеваемость детей ОСО составила 95,7 случая на 1000 человек (95% ДИ: 77,2–117,4) в целом, 105,5 случая (95% ДИ: 78,3–139,0) у детей ≤2 лет и 63,6 случая (95% ДИ: 43,2–90,3) у детей в возрасте 3–5 лет [6]. Согласно исследованию Р.С. Козлова и соавт. (2017), проведенному в Барнауле, Екатеринбурге и Мурманске, клинически подтвержденная заболеваемость ОСО среди детей в возрасте до 5 лет составляет 18,6 случая на 100 человеко-лет, при этом средняя частота случаев подозрения на ОСО составляет 64,2 на 100 человеко-лет [7].
Средний отит и сопутствующая воспалительная патология полости носа, носоглотки, околоносовых пазух не только имеют много общих патогенетических аспектов, но и часто оказываются коморбидными, особенно у детей. Эпидемии острых респираторных вирусных инфекций способствуют развитию тяжелых форм ОСО и ассоциированных с ними тяжелых осложнений [8]. Своевременное оказание медицинской помощи детям с ОСО, назначение комплексной терапии, направленной на эрадикацию инфекционного процесса в среднем ухе и сопутствующего воспаления верхних дыхательных путей, являются профилактикой неблагоприятного течения заболевания [9].
Национальная медицинская ассоциация оториноларингологов России рекомендует в составе комплексной терапии ОСО, наряду с разгрузочной, системной противовоспалительной и антибактериальной терапией, применение топической терапии (ушные капли) препаратами, содержащими неопиоидный анальгетик феназон и местный анестетик лидокаин на доперфоративной стадии [10]. На отечественном фармацевтическом рынке имеются несколько брендов ушных капель, содержащих указанные лекарственные препараты, однако исследования, посвященные объективной оценке их клинического эффекта, в настоящее время отсутствуют.
Цель исследования: оценить сравнительную эффективность, переносимость и безопасность применения лекарственных препаратов, содержащих феназон и лидокаин, в местной терапии острого среднего отита у детей.
Материал и методы
В клиническое исследование были включены 30 детей (17 (56,7%) мальчиков и 13 (43,3%) девочек) в возрасте от 3 до 14 лет с ОСО на доперфоративной стадии заболевания.
Включенные в исследование дети были рандомизированы на 2 группы по 15 человек в соответствии с планом рандомизации.
Группа 1: 15 пациентов с диагнозом ОСО, которые получали стандартную терапию + препарат (Лоротокс®), содержащий феназон и лидокаин, капли ушные для местного применения, согласно инструкции по применению препарата.
Группа 2: 15 пациентов, с диагнозом ОСО, которые получали стандартную терапию + препарат сравнения импортного производства (Отипакс®), содержащий феназон и лидокаин,капли ушные для местного применения, согласно инструкции по применению препарата.
Стандартную терапию проводилисогласно клиническим рекомендациям «Острый средний отит» от 2016 г.
Основные группы использованных лекарственных препаратов(показания к назначению препаратов определял ЛОР-врач):
разгрузочные (интраназальные): ирригационно-
элиминационные — промывание носа с использованием изотонического раствора хлорида натрия или морской воды (туалет носа у маленьких детей заключался в принудительном удалении отделяемого из носа); сосудосуживающие средства (деконгестанты) в рекомендуемых концентрациях для детей; интраназальные глюкокортикостероидные препараты; муколитические, секретолитические, секретомоторные (особенно у маленьких детей при невозможности удалить густой назальный секрет); топические антибактериальные;
системные для купирования болевого синдрома: нестероидные противовоспалительные средства (НПВС); дозы приема у детей: парацетамол 10–15 мг/кг 3–4 р./сут, ибупрофен 8–10 мг/кг 1 р./сут; НПВС являлись обязательным компонентом в комплексном лечении ОСО.
Кроме того, стандартная терапия ОСО включала:
рефлекторное воздействие на слизистую оболочку среднего уха (согревающий компресс), другие физиопроцедуры, согласно рекомендациям физиотерапевта;
мероприятия, направленные на восстановление функции слуховой трубы.
Включенные в исследование пациенты совершили 3 визита к ЛОР-врачу.
1-й визит: включение в исследование, подписание информированного согласия, сбор анамнестических данных (предшествующее отиту ОРВИ), ЛОР-обследование, назначение лечения, выдача анкеты для ведения дневника пациента.
2-й визит (5–8-е сут): клиническая оценка состояния больного, оценка жалоб, локального статуса, переносимости препарата, наличие побочных эффектов.
3-й визит (10–14-е сут): клиническая оценка состояния больного, оценка жалоб, локального статуса, переносимости препарата, сбор данных из анкеты пациента.
Выясняли, как пациент и его родители выраженность симптомов заболевания в сравнении с желаемым (асимптомным) состоянием по модифицированной 10-балльной визуальной аналоговой шкале (ВАШ) от 0 — «очень хорошо» до 10 — «очень плохо». Оценивали следующие признаки: слабость, недомогание, выраженность боли в ухе, снижения слуха, аутофонии, шума в ухе, головокружения, качество жизни.
Тяжесть клинического состояния пациентов с ОСО на доперфоративной стадии оценивали по 3-балльной системе — от 0 до 3 баллов. Оценивали в баллах следующие клинические признаки:
степень втянутости барабанной перепонки: 0 — не втянута, 1 — втянута незначительно, 2 — умеренно, 3 — выраженно;
степень утолщения барабанной перепонки: 0 — не утолщена, 1 — утолщена незначительно, 2 — умеренно, 3 — выраженно;
степень сглаженности опознавательных знаков барабанной перепонки: 0 — нет, 1 — сглажена незначительно, 2 — умеренно, 3 — выраженно;
степень инъекции сосудов барабанной перепонки: 0 — нет, 1 — инъецирована незначительно, 2 — умеренно, 3 — выраженно;
степень гиперемии барабанной перепонки: 0 — нет, 1 — выражена незначительно, 2 — умеренно, 3 — значительно;
степень ограничения подвижности барабанной перепонки: 0 — нет, 1 — ограничена незначительно, 2 — умеренно, 3 — значительно;
степень нарушения слуха при исследовании шепотной речью: 0 — 6 м, 1 — 4–5 м, 2 — 2–3 м, 3 — 1 м;
результаты термометрии тела: 0 — нормальная температура, 1 — субфебрильная температура, 2 — повышение температуры не выше 38 °С, 3 — повышение температуры выше 38 °С;
симптомы общей интоксикации: 0 — нет, 1 — незначительные симптомы, 2 — умеренные, 3 — выраженные.
Эффективность исследуемых лекарственных препаратов, содержащих феназон и лидокаин, в местной терапии ОСО оценивали на основании сравнения клинических показателей в 2 группах детей.
Все клинические данные, входящие в дизайн исследования, заносились в индивидуальную регистрационную карту пациента. Врач также исследовал анкеты пациента с данными субъективного статуса. Для интерпретации результатов исследования были использованы методы описательной и аналитической статистики.
Оценивали безопасность исследуемых лекарственных препаратов, содержащих феназон и лидокаин, в местной терапии ОСО по нежелательным явлениям, которые отмечали в ходе исследования и заносили в индивидуальную регистрационную карту пациента.
В целях объективной и комплексной оценки жалоб пациентов, клинических проявлений заболевания, статуса ЛОР-органов, а также для удобства последующей статистической обработки и интерпретации указанные в дневниках пациента баллы и данные клинического наблюдения были суммированы относительно визитов пациента к врачу или сроков от начала лечения (1–10-й день).
Статистический анализ. При обработке данных использовали программный пакет IBM SPSS Statistics 22 (Armonk, NY, USA),методы описательной и аналитической статистики. Рассматривали как категориальные (наличие или отсутствие изучаемого фактора, пол), так и количественные данные (суммы баллов из дневников пациента и клинического наблюдения). Анализируемые параметры категориальных данных представлены в виде долей и частот от общего числа исследуемых (%). Параметры количественных данных в исследовании представлены в виде медианы (Me) и 25%, 75% квартилей [Q25; Q75], поскольку они не соответствовали закону нормального распределения согласно критерию Shapiro — Wilk, тесту Levene.
Оценка значимости различий медиан количественных показателей в группах исследования проводилась при помощи U-критерия Mann — Whitney. Оценку эффекта лечения при повторных измерениях проводили методом сравнительного статистического анализа сумм баллов из дневников пациентов и протоколов клинического наблюдения. Различия в субъективном и объективном статусах пациентов на фоне проводимой терапии выявляли с использованием непараметрического критерия χ2(2) Friedman с критическим уровнем значимости 0,05. С целью уточнения скорости наступления лечебного эффекта проводили апостериорные множественные попарные сравнения балльных и термометрических показателей (post hoc анализ) с использованием непараметрического Z-критерия Wilcoxon с поправкой Bonferroni для критического уровня значимости: р/m (m — количество возможных гипотез (сравнений)), критический уровень с учетом поправки Bonferroni составил 0,017. Для 10 же повторных наблюдений из дневников пациента, обусловливающих 20 возможных сравнений, за критический уровень значимости принималось значение в 0,0025.
Результаты исследования
Пациенты в исследуемых группах по возрастному, гендерному составу статистически значимо не различались (табл. 1).

Все пациенты прошли лечение в соответствии с установленным протоколом, показали удовлетворительный комплаенс. Отмечали очень хорошую переносимость всех применяемых препаратов, в т. ч. феназона и лидокаина, при местном применении. В ходе наблюдения за пациентами нежелательных явлений при местном применении феназона и лидокаина не зарегистрировано.
Динамика клинического статуса пациентов
Примененное в исследовании лечение ОСО на доперфоративной стадии демонстрировало достижение статистически значимой положительной динамики со стороны жалоб и клинического статуса детей обеих групп при повторных осмотрах ЛОР-врачом (табл. 2, 3). Межгрупповые различия не выявлены (p>0,001), различия в результатах между визитами внутри групп достоверны (p<0,001).
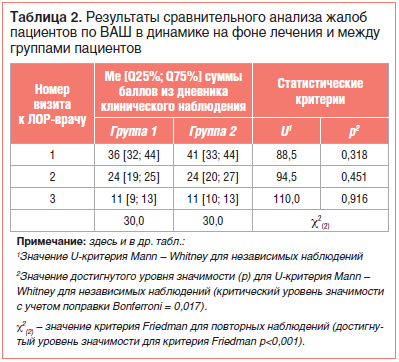
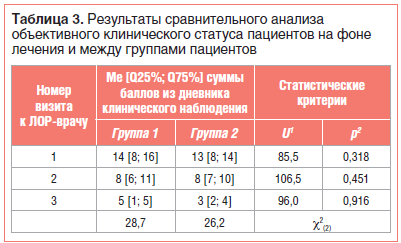
Апостериорное попарное сравнение балльных показателей повторной оценки жалоб и клинического статуса пациентов относительно номера визита к ЛОР-врачу выявило отчетливую равномерную положительную динамику начиная со 2-го визита в обеих группах пациентов. Статистически значимых различий при групповом попарном сравнении балльных показателей жалоб и клинического статуса пациентов относительно номера визита не выявлено (см. табл. 2, 3; рис. 1, 2).
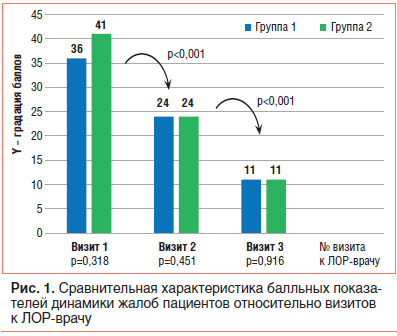
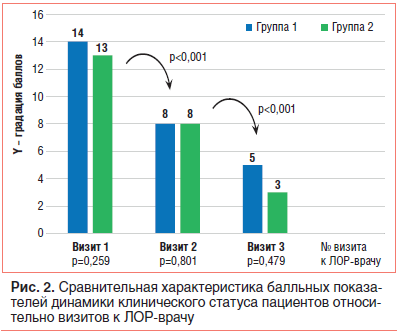
Оценка результатов лечения детей с неперфоративным ОСО на основании динамического сравнения суммированных балльных показателей из их дневников (субъективный статус) выявила статистически значимое уменьшение выраженности клинических проявлений основного заболевания на фоне проводимого лечения в обеих группах (табл. 4).
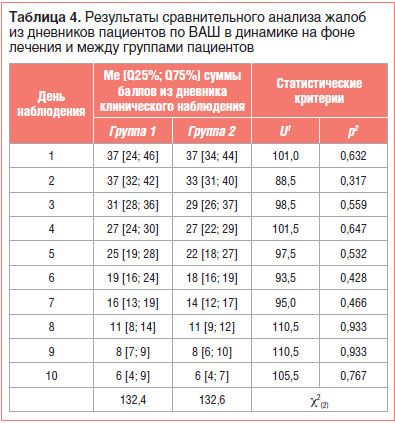
Статистически значимых различий при групповом попарном сравнении балльных показателей субъективного статуса пациентов относительно дня от начала лечения ОСО не выявлено (см. табл. 4; рис. 3).

Оценка результатов термометрии у детей с ОСО на основании динамического сравнения суммированных балльных показателей из их дневников (субъективный статус) выявила статистически значимое уменьшение выраженности лихорадки на фоне проводимого лечения в обеих группах без статистически значимых различий между ними (табл. 5).

Выводы
Применение лекарственных препаратов, содержащих феназон и лидокаин, в местной терапии ОСО на доперфоративной стадии (стадия острого евстахиита, стадия острого катарального или экссудативного воспаления) у детей показало свою клиническую эффективность, которая подтверждена клиническими специализированными оториноларингологическими исследованиями, а также на основании дневников, заполненных родителями на основе субъективных ощущений пациентов. Эффективность местной противовоспалительной терапии сохранялась на протяжении всего периода наблюдения. Эффективность противовоспалительного и обезболивающего эффекта доказана с использованием современных методов медицинской статистики. При этом различия клинических показателей и показателей, выраженных в баллах, в группах исследования не были статистически значимы. Побочных и нежелательных эффектов терапии у обследованных 30 пациентов не выявлено.
Результаты сравнительного анализа объективных и субъективных клинических результатов лечения пациентов 1-й и 2-й групп наблюдения свидетельствуют об одинаковой эффективности препаратов Лоротокс® и импортного аналога (Отипакс®), капли ушные для местного применения, содержащих феназон и лидокаин, в местной терапии ОСО у детей.
Таким образом, препараты, содержащие феназон и лидокаин, капли ушные для местного применения, являются безопасным и эффективным средством в составе комплексного лечения детей с ОСО на доперфоративной стадии, что позволяет включать их в комплексную терапию. Своевременное начало комплексной терапии, особенно в детском возрасте, снижает риск развития мастоидита и других локальных и системных осложнений [8–10].
Источник