Клинические рекомендации по внебольничной пневмонии 2015 год


Российское респираторное общество Межрегиональное педиатрическое респираторное общество
Федерация педиатров стран СНГ Московское общество детских врачей
ВНЕБОЛЬНИЧНАЯ
ПНЕВМОНИЯ У ДЕТЕЙ
Клинические рекомендации
УДК 616.24-002-053.2 ББК 57.334.12
В60
В60 Внебольничная пневмония у детей. Клинические рекомендации. — Москва : Ори- гинал-макет, 2015. — 64 с.
ISBN 978-5-990-66034-2
УДК 616.24-002-053.2 ББК 57.334.12
Научное издание
ВНЕБОЛЬНИЧНАЯ ПНЕВМОНИЯ У ДЕТЕЙ. КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
Оригинал-макет подготовлен компанией ООО «Оригинал-макет» www.o-maket.ru; тел.: (495) 726-18-84 Санитарно-эпидемиологическое заключение
№ 77.99.60.953.Д.004173.04.09 от 17.04.2009 г. Подписано в печать 20.08.2015. Формат 70×100 1/16. Печать офсетная. Печ. л. 4,0. Тираж 21 100 экз. Заказ №
ISBN 978-5-990-66034-2 | © ООО «Оригинал-макет», оформление, 2015 |
Руководитель проекта:
Председатель правления Российского респираторного общества, академик РАМН, профессор А.Г. Чучалин
Координационный совет:
профессор, д.м.н. Геппе Н. А., профессор д.м.н. Розинова Н.Н., профессор, д.м.н. Волков И.К., профессор, д.м.н. Козлова Л.В., профессор, д.м.н. Малахов А.Б., профессор, д.м.н. Манеров Ф.К., профессор д.м.н. Мизерницкий Ю.Л.
Эксперты: Абдрахманова С.Т. (Астана), Антипкин Ю.Г. (Киев), Ашерова И.К. (Ярославль), Балева Л.С. (Москва), Баскакова А.Е. (Кострома), Бойцова Е.В. (С.-Петербург), Богорад А.Е. (Москва), Больбот Ю.К. (Днепропетровск), Бондарь Г.Н. (Владивосток), Буйнова С.Н. (Иркутск), Вавилова В.П. (Кемерово), Василевский И.В. (Минск), Гаймоленко И.Н. (Чита), Геппе Н.А. (Москва), Горелов А.В. (Москва), Донос А.А. (Кишинев), Дронов И.А. (Москва), Елкина Т.Н. (Новосибирск), Ермакова И.Н. (Тверь), Ермакова М.К. (Ижевск), Заболотских Т.В. (Благовещенск), Ильенкова Н.А. (Красноярск), Камаев А.В. (С.-Петербург), Капранов Н.И. (Москва), Кожевникова Т.Н. (Тула), Козлова Л.В. (Смоленск), Колесникова С.М. (Хабаровск), Колосова Н.Г. (Москва), Кондратьева Е.И. (Москва), Кондюрина Е.Г. (Новосибирск), Копилова Е.Б. (Иваново), Кострова В.П. (Махачкала), Косякова Н.И. (Пущино), Кулагина В.В. (Самара), Лапшин В.Ф. (Киев), Лев Н.С. (Москва), Лютина Е.И. (Новокузнецк), Маланичева Т.Г. (Казань), Малахов А.Б. (Москва), Манеров Ф.К. (Новокузнецк), Мельникова И.М. (Ярославль), Мещеряков В.В. (Нижневартовск), Мизерницкий Ю.Л. (Москва), Михалев Е.В. (Томск), Мозжухина Л.И. (Ярославль), Мокина Н.А. (Самара), Неретина А.Ф. (Воронеж), Олехнович В.М. (Сургут), Павлинова Е.Б. (Сургут), Побединская Н.С. (Иваново), Постников С.С. (Москва), Розинова Н.Н. (Москва), Романенко В.А. (Челябинск), Рывкин А.И. (Иваново), Саввина Н.В. (Якутск), Савенкова М.С. (Москва), Самсыгина Г.А. (Москва), Середа Е.В. (Москва), Скачкова М.А. (Оренбург), Скучалина Л.Н. (Астана), Соколина И.А. (Москва), Сорока Н.Д. (C.-Петербург), Спичак Т.В. (Москва), Таточенко В.К. (Москва), Тришина С.В. (Симферополь), Тутуева Л.А. (Севастополь), Узакбаев К.А. (Бишкек), Узунова А.Н. (Челябинск), Файзуллина Р.М. (Уфа), Федоров И.А. (Челябинск), Хачатрян Л.Г. (Москва), Холодок Г.Н. (Хабаровск), Царькова С.А. (Екатеринбург), Чепурная М.М. (Ростов-на-Дону), Черная Н.Л. (Ярославль), Шабалов Н.П. (С.-Петербург), Шамсиев Ф.М. (Ташкент), Шуляк И.П. (Екатеринбург).
ВВЕДЕНИЕ
Внебольничная пневмония (ВП) являются актуальной проблемой для педиатрической практики. В последние годы отмечается рост заболеваемости ВП у детей, относительно высокой остается смертность от этого заболевания. В реальной практике, особенно в амбулаторных условиях, серьезными проблемами являются ранняя диагностика и рациональная терапия пневмонии у детей.
В 2010 году при участии 65 экспертов из России и стран СНГ была создана научно-практическая программа «Внебольничная пневмония у детей: распространенность, диагностика, лечение и профилактика» [1], которая издавалась с небольшими переработками в 2011
и2012 годах. В программе были резюмированы накопленные данные по вопросам этиологии, патогенеза, эпидемиологии, диагностики
илечения ВП у детей.
За последние 5 лет было проведено и представлено в мировой научной литературе большое число клинических и эпидемиологических исследований, касающихся пневмонии. К сожалению, в отечественной литературе этой проблеме уделяется недостаточно внимания. В 2013 году Министерством здравоохранения Российской Федерации были приняты новые стандарты медицинской помощи при пневмонии и «Порядок оказания медицинской помощи населению по профилю «пульмонология»». С 2014 года в Национальный календарь профилактических прививок России включена вакцинация против пневмококковой инфекции. В связи с вышесказанным назрела необходимость пересмотра ряда позиций, относительно ВП у детей и создание нового экспертного документа, отражающего современные клинические рекомендации.
Основное внимание в данном документе уделено практическим вопросам диагностики и терапии ВП у детей, и в частности особенностям ведения детей в амбулаторных условиях, включены данные по особенностям ВП у детей с ВИЧ-инфекцией, ДЦП, муковисцидозом. Книга предназначена для педиатров, врачей общей практики, пульмонологов, клинических фармакологов, реаниматологов, а также преподавателей медицинских вузов.
При подготовке клинических рекомендаций авторы пытались строить рекомендации по диагностике и лечению на основе данных доказательной медицины (таблица 1). Однако необходимо учитывать, что
внастоящее время доказательная база в отношении методов лечения
впедиатрии, в том числе по АБТ явно недостаточна, что связано с этическими и деонтологическими проблемами. Также следует учитывать, что эффективность этиотропной терапии пневмонии принципиально зависит от чувствительности возбудителей к АБП, которая имеет значительные региональные особенности и подвержена существенным изменениям.
5
Таблица 1 Категории доказательств для обоснования применения
в клинических рекомендациях
Категория | Источник | Определение доказательств |
доказательств | ||
A | Рандомизированные | Доказательства основаны на хорошо сплани- |
контролируемые | рованных рандомизированных исследовани- | |
исследования | ях, проведенных на достаточном количестве | |
пациентов, необходимом для получения | ||
достоверных результатов. Могут быть | ||
обоснованно рекомендованы для широкого | ||
применения | ||
B | Рандомизированные | Доказательства основаны на рандомизи- |
контролируемые | рованных контролируемых исследованиях, | |
исследования | однако количество включенных пациентов | |
недостаточно для достоверного статистиче- | ||
ского анализа. Рекомендации могут быть рас- | ||
пространены на ограниченную популяцию | ||
C | Нерандомизированные | Доказательства основаны на нерандомизи- |
клинические | рованных клинических исследованиях или | |
исследования | исследованиях, проведенных на ограничен- | |
ном количестве пациентов | ||
D | Мнение экспертов | Доказательства основаны на выработанном |
группой экспертов консенсусе по определен- | ||
ной проблеме |

Глава 1 ОПРЕДЕЛЕНИЕ И КЛАССИФИКАЦИЯ
ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ У ДЕТЕЙ
1.1. Определение
Пневмония — острое инфекционное заболевание, различное по этиологии (преимущественно бактериальное), характеризующееся очаговыми поражениями легких с внутриальвеолярной экссудацией, что проявляется выраженными в различной степени интоксикацией, респираторными нарушениями, локальными физикальными изменениями со стороны легких и наличием инфильтративной тени на рентгенограмме грудной клетки.
Внебольничная пневмония (домашняя, амбулаторная) — это пневмония, развившаяся вне больницы или в первые 72 часа госпитализации.
1.2.Классификация
Всоответствии с Международной классификацией болезней, травм
ипричин смерти 10–го пересмотра (МКБ-10) и «Классификацией клинических форм бронхолегочных заболеваний у детей» [2] выделяют следующие формы пневмонии:
1. По этиологии:
•бактериальная (в то числе, вызванная атипичными бактериями);
•вирусная;
•грибковая;
•паразитарная;
•смешанная.
Классификация по этиологии положена в основу МКБ 10 пересмотра (приложение 1). Однако, широкое использование этиологической классификации пневмонии невозможно, поскольку верификация этиологии ВП отсутствует у большинства пациентов, а клинические симптомы малоинформативны для этиологической диагностики.
2.По морфологии:
•очаговая — один или несколько очагов пневмонической инфильтрации размером 1–2 см;
•очагово-сливная (псевдолобарный инфильтрат) — неоднородная массивная пневмоническая инфильтрация, состоящая из нескольких очагов. Может осложняться деструктивными процессами и экссудативным плевритом;
•сегментарная — границы повторяют анатомические границы одного сегмента;
7
•полисегментарная — границы инфильтрации повторяют анатомические границы нескольких сегментов. Часто протекает с уменьшением размеров пораженного участка легкого (ателектатический компонент);
•лобарная (долевая) — инфильтрация охватывает долю легкого. Вариантом течения долевой пневмонии является крупозная пневмония;
•интерстициальная — наряду с негомогенными инфильтратами легочной паренхимы имеются выраженные, иногда преобладающие изменения в интерстиции легких. Редкая форма пневмонии, которая развивается у больных с ИДС.
3.По течению:
•острая — длительность до 6 недель;
•затяжная — длительность более 6 недель.
4.По тяжести:
•средней тяжести;
•тяжелая.
5.По развившимся осложнениям:
•плевральные осложнения — плеврит;
•легочные осложнения — полостные образования, абсцесс;
•легочно-плевральные осложнения — пневмоторакс, пиопневмоторакс;
•инфекционно-токсические осложнения — бактериальный шок [2, 3].
Глава 2 ЭПИДЕМИОЛОГИЯ ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ
2.1.Заболеваемость внебольничной пневмонией
С2011г. ВП включена в перечень инфекционных и паразитарных заболеваний, подлежащих регистрации и государственному учету в Российской Федерации, а статистические показатели заболеваемости вносятся Федеральной службой по надзору в сфере защиты прав потребителей
иблагополучия человека в «Сведения об инфекционных и паразитарных заболеваниях» (до 2010 г. Минздравом РФ представлялись показатели заболеваемости в целом по внебольничной и госпитальной пневмонии). Данные по заболеваемости ВП представлены в табл. 2. Правила регистрации случаев заболевания ВП представлены в приложении 2.
Таблица 2 Динамика показателей заболеваемости ВП у детей и подростков в РФ [4]
Показатели | 2011 г. | 2012 г. | 2013 г. | 2014 г. | |
У детей в возрасте до 17 лет | абсолютное число | 139 016 | 168 391 | 190 711 | 181 313 |
включительно | на 100 тыс. населения | 534,3 | 642,5 | 722,8 | 678,7 |
У детей в возрасте до 15 лет | абсолютное число | 129 055 | 154 160 | 176 093 | 171 604 |
включительно | на 100 тыс. населения | 607,4 | 711,5 | 800,9 | 762,3 |
В2014 г. среди всего населения Российской Федерации из 507031 случая заболеваний ВП (заболеваемость 354,1 на 100 тыс. населения) на детей и подростков до 17 лет пришлось 181313 случаев (заболеваемость 678,7 на 100 тыс. населения), из них на детей до 15 лет 171604 случая (заболеваемость 762,3 на 100 тыс. населения) [4]. Таким образом, заболеваемость ВП среди детей до 15 лет более чем в 2 раза превышает заболеваемость для населения в целом.
Эпидемиологические исследования показывают, что в течение года заболеваемость ВП минимальная в июле–сентябре, повышается в октя- бре–декабре, достигает максимума в январе–апреле и снижается в мае– июне. Заболеваемость ВП коррелирует с сезонным повышением уровня ОРВИ [5]. Вспышки микоплазменной ВП характерны для закрытых коллективов и отмечаются каждые 3–5 лет [1].
Вряде регионов РФ заболеваемость ВП регистрировалась и до 2010 г.
Вг. Новокузнецке за 24-летний период наблюдения (1990–2013 гг.) заболеваемость ВП среди детей составляла от 210 до 890 на 100 тыс. населения (2,1–8,9‰), среди подростков — от 140 до 840 на 100 тыс. населения (1,4–8,4‰). Максимальная заболеваемость ВП во все годы наблюдалась у детей в возрасте 1–3 лет — от 465 до 1356 на 100 тыс населения (рис. 1) [6].
9
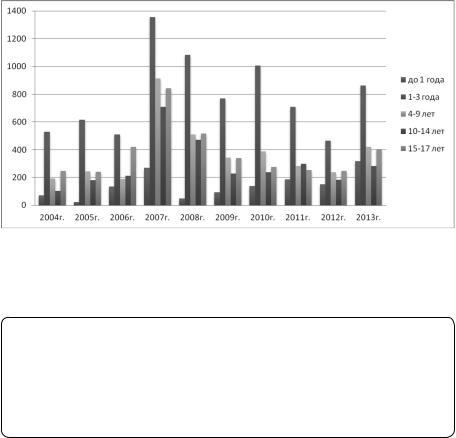
Рис. 1. Заболеваемость внебольничной пневмонией у детей разного возраста
вг. Новокузнецке за 10-летний период [6]
2.2.Смертность от внебольничной пневмонии
По данным ВОЗ пневмония является главной причиной детской смертности во всем мире. Среди причин летальности у детей до 5 лет на ее долю приходится 17,5%, что ежегодно в мире составляет около 1,1 млн смертельных случаев (это больше, чем СПИД, малярия и корь вместе взятые). При этом 99% летальных случаев от пневмонии у детей до 5 лет приходятся на слабо и средне развитые страны мира [7].
Вглобальном исследовании было установлено, что в 2010 г. летальность
всвязи с тяжелыми острыми инфекциями нижних дыхательных путей у госпитализированных детей в возрасте до 5 лет в развивающихся странах была почти в 4 раза выше, чем в развитых (2,3% и 0,6%, соответственно) [8].
По данным Минздрава РФ болезни органов дыхания у детей в возрасте 0–17 лет занимают третье место в структуре причин смерти после внешних причин и пороков развития. В РФ в последние годы произошло значительное снижение смертности от пневмонии детей первого года жизни: с 16,1 в 1995 г. до 2,7 в 2012 г. на 10 000 родившихся живыми (при этом, в 24% пневмония выступает не основной, а конкурирующей причиной смерти больных). Данные о смертности от пневмонии по регионам РФ имеют значительный разброс показателей — от 0 до 13,7 на 10 000 (в 2009г.) [1, 4, 9].
Фоновые факторы риска летального исхода от пневмонии у детей [9]:
• возраст до 5 лет и мужской пол;
• врожденные и хронические заболевания;
• позднее обращение за медицинской помощью;
• позднее поступление в стационар;
• гестационный возраст при рождении меньше 28 недель.
Источник
ММА имени И.М. Сеченова
Внебольничная пневмония (ВП) — острое инфекционное воспаление альвеол, возникающее вне стационара и проявляющееся клиническими и (или) рентгенологическими признаками, не связанными с другими причинами
Доминирующие возбудители ВП
— Streptococcus pneumoniae
— Haemophilus influenzae
— Mycoplasma pneumoniae
— Chlamydia pneumoniae
— Legionella pneumophilla
— Staphylococcus aureus
— анаэробы.
Классификация ВП
- Пневмонии у больных без сопутствующей патологии
- Пневмонии на фоне тяжелых соматических заболеваний
- Аспирационные пневмонии.
Клиническая симптоматика пневмоний
— респираторные симптомы (кашель, одышка, боли в груди, крепитация, бронхиальное дыхание, притупление перкуторного звука),
— симптомы интоксикации (лихорадка, ознобы, головная боль, общемозговая симптоматика и др.),
— декомпенсация сопутствующей патологии (ХОБЛ, сердечная недостаточность, сахарный диабет и др.).
Дополнительные диагностические признаки
— лабораторные (нейтрофильный лейкоцитоз или лейкопения),
— рентгенологические (легочный инфильтрат, плевральный выпот),
— бактериоскопия мокроты при окраске по Граму,
— серологическая диагностика (антитела к микоплазме и хламидиям).
Окраска мокроты по Граму является важным ориентиром для выбора первоначального антибиотика с учетом «грам-принадлежности» микроорганизмов. Особенно целесообразным следует считать бактериоскопию и посев мокроты, содержащей достаточное количество нейтрофилов в условиях стационара. Отрицательный результат при окраске мокроты по Граму не всегда свидетельствует об отсутствии микроорганизмов в мокроте и может быть обусловлен недостаточным их количеством (менее 104). Если в одном поле зрения обнаруживается около 10 микроорганизмов, то это означает, что их количество составляет не менее 105 и приближается к диагностическому титру.
Серологическая диагностика может иметь значение при верификации атипичных микроорганизмов (обычно ретроспективной) на основании уровня IgG и IgM антител через 2-3 недели.
Формулировка диагноза пневмонии должна отражать:
— Нозологическую форму (внебольничная или внутрибольничная),
— этиологический вариант ВП (ориентировочный или верифицированный),
— фоновую патологию (характер, активность),
— локализацию и распространенность легочного воспаления (по данным рентгенологического исследования),
— наличие осложнений (легочных и внелегочных),
— тяжесть пневмонии,
— фазу заболевания (разгар, разрешение),
— течение (обычное, затяжное).
Принятие ключевых решений при ведении больного ВП
— Определение места лечения (амбулаторное или стационарное),
— выбор первоначального антибактериального препарата (АП),
— оценка эффективности АП через 48-72 часа и принятие решения о дальнейшей тактике лечения,
— продолжительность антибактериальной терапии (АТ),
— принятие решения о переходе с парентерального на оральный путь введения АП,
— необходимость и показания к симптоматической терапии.
В нетяжелых случаях лечение может проводиться амбулаторно. Показаниями для госпитализации являются:
— возраст старше 65 лет,
— наличие тяжелой сопутствующей патологии (ХОБЛ, сердечная недостаточность, сахарный диабет, иммунодефицитные состояния и др.),
— невозможность адекватного ухода и выполнения врачебных назначений в домашних условиях,
— предпочтение стационарного лечения больным или членами его семьи,
— наличие одного из критериев тяжелого течения пневмонии,
— неэффективность антибактериальной терапии в течение 72 часов.
Антибактериальные препараты, назначаемые при внебольничных пневмониях
— Аминопенициллины (амоксициллин),
— защищенные пенициллины (амоксициллин/клавулановая кислота, ампициллин/сульбактам),
— макролиды (эритромицин, кларитромицин, спирамицин, мидекамицин и др.),
— цефалоспорины I-III поколений,
— фторхинолоны (ципрофлоксацин, моксифлоксацин),
— линкозамины (клиндамицин, линкомицин).
Требования к АП, назначаемым для лечения пневмонии
— Активность против основных возбудителей пневмонии,
— оптимальная концентрация в легочной ткани и альвео лярных макрофагах,
— хорошая биодоступность АП при назначении внутрь,
— отсутствие клинически значимого взаимодействия с другими медикаментами,
— длительный период полувыведения,
— минимальная резистентность микроорганизмов,
— относительно низкая токсичность и безопасность,
— наличие препарата в различных лекарственных формах.
Продолжительность АТ
Продолжительность АТ внебольничной пневмонии определяется различными факторами, в том числе ответом на терапию, тяжестью пневмонии, наличием осложнений, характером возбудителя (этиологическим вариантом). В случаях неосложненного течения пневмонии, вызванной S. pneumoniae, H. Influenzae, длительность АТ не должна превышать, как правило, 7-10 дней. При пневмонии, вызванной внутриклеточными возбудителями (Legionella, Mycoplasma), а также у больных с наличием осложнений (абсцесс) продолжительность лечения может достигать 21 дня. Рентгенологическое разрешение пневмонии, нормализация СОЭ происходят в более поздние сроки, чем исчезновение признаков интоксикации и респираторной симптоматики.
С целью обеспечения большей комфортности лечения и снижения затрат на лечение при наступлении клинического эффекта в течение 48-72 часов возможен переход с парентерального на оральный путь введения АП. Требования к переходу с парентерального на оральный путь введения антибиотика:
— наличие антибиотика в оральной и парентеральной форме,
— эффект от парентерально вводимого антибиотика,
— стабильное состояние больного,
— возможность приема препаратов внутрь,
— отсутствие патологии со стороны кишечника,
— высокая биодоступность орального антибиотика.
Особые ситуации при лечении больных пневмонией
— Беременность,
— наличие сопутствующей патологии (печень, почки и др.),
— гиперчувствительность к различным антибактериальным препаратам,
— пневмонии, вызванные т.н. атипичными возбудителями,
— осложненные пневмонии,
— пневмонии тяжелого течения с неустановленным возбудителем,
— пневмонии затяжного течения,
— отсутствие эффекта от первоначального АП.
При выборе АП для лечения пневмонии у беременных ошибочно назначение фторхинолонов, клиндамицина, метронидазола. Кроме того, с осторожностью должны назначаться аминогликозиды, ванкомицин, имипенем.
Наличие сопутствующей патологии с функциональными нарушениями со стороны почек и печени создает сложности в проведении АТ, что может приводить к ошибкам в выборе АП, его дозировки, путях введения, длительности АТ и т.д. При этом ошибочно назначение потенциально нефротоксичных АП (аминогликозиды, карбапенемы) без корректировки дозы у больных с сопутствующей почечной недостаточностью. Опасно также в подобных ситуациях сочетание АП, обладающих нефротоксическими свойствами (аминогликозиды и цефалоспорины, за исключением цефоперазона). При наличии у больного почечной недостаточности следует отдавать предпочтение выбору АП с преимущественно внепочечным выведением препарата с желчью или путем метаболизма в печени (цефоперазон, макролиды, клиндамицин, пефлоксацин). Особенно следует учитывать наличие сопутствующей, нередко множественной патологии с функциональными нарушениями органов и систем у больных пожилого и старческого возраста. Возрастное снижение показателей клубочковой фильтрации наряду с высокой частотой нефроангиосклероза у пожилых должны быть одним из факторов, влияющих на выбор АП. Наличие патологии со стороны желудочно-кишечного тракта (в частности, нарушения кишечного всасывания) ограничивает возможности назначения АП внутрь и проведение ступенчатой терапии. Дополнительные трудности при выборе АП и оценке риска побочных нежелательных эффектов могут возникать у больных, получающих по поводу сопутствующей патологии различные лекарственные препараты (теофиллины, сердечные гликозиды, петлевые диуретики, соли кальция и др.). В подобных ситуациях следует отдавать предпочтение АП с минимальным лекарственным взаимодействием.
При наличии достоверно установленной гиперчувствительности к пенициллину не следует назначать другие b-лактамные АП (цефалоспорины, карбопенемы). Альтернативными АП могут быть фторхинолоны, макролиды. Однако нередко за «аллергию на антибиотики» могут приниматься реакции другого происхождения (сосудистые, вегетативные и др.), в связи с чем следует критически оценивать указания больных на такую «непереносимость» и более тщательно анализировать имеющуюся ситуацию. Вместе с тем опасны внутрикожные пробы на АП, поскольку при этом существует такая же опасность тяжелых анафилактических реакций.
Пневмонии, вызываемые L. pneumophilla, Mycoplasma pneumoniae, Chlamydia pneumoniae (т.н. атипичные пневмонии), имеют целый ряд эпидемиологических и клинических особенностей, что вызывает не только трудности диагностики, но и АТ данного этиологического варианта пневмоний. Особенностями атипичных пневмоний являются следующие:
— основные возбудители — Mycoplasma, Chlamidia, Legionella,
— внутриклеточная локализация возбудителей,
— частая внелегочная симптоматика,
— особые эпидемиологические ситуации,
— симптоматика ОРВИ в дебюте заболевания (Mycoplasma),
— невозможность выявления возбудителей в мокроте,
— специфические серологические данные,
— неэффективность b-лактамных антибиотиков,
— эффективность макролидов, тетрациклинов, фторхинолонов.
Тяжесть пневмонии. Основные проблемы внебольничных пневмоний тяжелого течения:
— декомпенсация сопутствующей патологии,
— трудности АТ,
— частое лечение в отделениях реанимации и интенсивной терапии,
— худший прогноз по сравнении с пневмониями более легкого течения,
— высокая летальность, особенно среди госпитализированных больных,
— высокая стоимость лечения.
Основные принципы лечения внебольничных пневмоний тяжелого течения:
— верификация степени тяжести пневмонии,
— обязательное лечение в стационаре,
— максимально быстрое начало АТ,
— назначение антибактериального препарата (препаратов), максимально перекрывающего вероятных возбудителей пневмонии,
— обязательное назначение препарата (препаратов) внутривенно,
— целесообразность комбинированной антибактериальной терапии,
— тщательное мониторирование состояния больного,
— своевременная смена препарата (препаратов) при отсутствии эффекта,
— использование ступенчатой АТ,
— адекватная симптоматическая и поддерживающая терапия.
Очевидны трудности в принятии решения о выборе АП у больных тяжелыми пневмониями, тем более что лечение тяжелых пневмоний должно начинаться как можно раньше. Следует ориентироваться на наиболее частые возбудители тяжелых пневмоний, которыми считаются S. pneumoniae, S. aureus, Enterobactericae, Legionella pneumophila. В то же время такие возбудители, как Mycoplasma pneumoniae, H. influenzae обычно не приводят к тяжелому течению заболевания. В условиях эмпирической АТ тяжелых пневмоний назначаемый АП должен перекрывать все вероятные этиологически значимые возбудители заболевания. Если при внебольничных пневмониях легкого течения можно ограничиться монотерапией — назначением аминопенициллинов (в том числе и защищенных) или макролидов, то при тяжелых пневмониях оправдана комбинированная АТ. Практически все клинические рекомендации по лечению тяжелых пневмоний включают цефалоспорины III поколения (цефотаксим, цефтриаксон) в сочетании с парентерально вводимыми макролидами (эритромицин, кларитромицин) или назначение защищенных пенициллинов (амоксициллин/клавулановая кислота) в сочетании с макролидами. Целесообразность комбинации b-лактамных антибиотиков с макролидами при лечении тяжелых пневмоний обусловлена вероятностью легионелезной пневмонии и трудностями ее этиологической верификации. При назначении комбинированной АТ цефалоспоринами III поколения в сочетании с макролидами летальность при внебольничной пневмонии (особенно среди больных пожилого возраста) ниже по сравнению с монотерапией цефалоспоринами III поколения. К настоящему времени имеется целый ряд исследований, свидетельствующих о клинической и бактериологической эффективности респираторных фторхинолонов (левофлоксацин, моксифлоксацин) в режиме монотерапии при лечении тяжелых пневмоний, сопоставимой с результатами сочетанной антибактериальной терапии цефалоспоринами или защищенными пенициллинами в сочетании с макролидами.
Пневмонии затяжного течения с замедленным разрешением
Факторы, определяющие затяжное рентгенологическое разрешение пневмонии:
— возраст старше 50 лет,
— наличие сопутствующей патологии (ХОБЛ, сахарный диабет, алкоголизм, опухоли и др.),
— тяжесть пневмонии,
— характер возбудителя (легионелла, хламидия).
Отсутствие эффекта от первоначального АП. Общепринятым сроком оценки эффективности АП считается 48-72 часа с момента его назначения. Критерием эффективности АП обычно является снижение или нормализация температуры тела больного, уменьшение признаков интоксикации. В тех случаях, когда лихорадка с самого начала заболевания не выражена или вообще отсутствует, приходится ориентироваться на другие признаки интоксикации (головная боль, анорексия, общемозговая симптоматика и т.д.), а также на отсутствие прогрессирования заболевания за период проводимого лечения. Продолжение АТ, несмотря на ее неэффективность, затягивает назначение другого, более адекватного АП, способствует прогрессированию легочного воспаления, возникновению осложнений, удлиняет сроки лечения, повышает риск возникновения побочных (токсических) эффектов АТ и развития антибиотикорезистентности.
В случаях неэффективности первоначального АП могут возникать трудности при выборе другого антибиотика. При отсутствии данных микробиологического исследования принцип выбора АП остается тем же самым — т.е. ориентировка на клиническую ситуацию с учетом неэффективности первоначального АП, что в известной степени должно быть дополнительным ориентиром выбора второго АП. Так, отсутствие эффекта от b-лактамных АП (пенициллины, цефалоспорины) у больного внебольничной пневмонией позволяет предполагать легионелезную или микоплазменную пневмонию (с учетом, разумеется, других признаков), что делает обоснованным назначение макролидов (эритромицин, спирамицин, кларитромицин и др.) или фторхинолонов (пефлоксацин, левофлоксацин).
Тактика ведения больных с затяжным течением пневмонии приведена на рисунке 1.
Рис. 1. Тактика при затяжном рентгенологическом разрешении пневмонии
Основными причинами неэффективности первоначального АП могут быть следующие:
— ошибочный диагноз пневмонии и наличие другого заболевания,
— неадекватный первоначальный АП,
— тяжелое течение пневмонии,
— наличие невыявленных осложнений,
— неадекватные доза, путь введения АП.
Одной из причин неэффективности лечения пневмонии могут быть неадекватные дозы АП, не создающие в крови концентрации, необходимой для эрадикации соответствующего возбудителя. Ошибки в выборе оптимальной дозы могут быть связаны с назначением как недостаточной разовой дозы, так и с неправильным режимом дозирования (недостаточная кратность введения). С учетом наличия у некоторых АП т.н. постантибиотического эффекта (способность препарата подавлять рост микроорганизмов даже при снижении уровня АП в крови ниже МПК) при назначении таких препаратов (тетрациклины, фторхинолоны, аминогликозиды) важна достаточная разовая доза, а интервалы между введениями могут быть более длительными. С другой стороны, b-лактамные АП (пенициллины, цефалоспорины I и II поколения), за исключением карбапенемов, практически лишены постантибиотического эффекта, в связи с чем для их оптимального действия гораздо важнее длительное поддержание в крови МПК, т.е. более частые (без пропусков) введения препарата.
Антибиотикорезистентность. Рациональная АТ пневмоний требует учета степени риска антибиотикорезистентности некоторых микроорганизмов, например, резистентности S. pneumoniae к пенициллину. К факторам риска пенициллинорезистентности S. pneumoniae относятся: возраст больных менее 7 лет и старше 60 лет, наличие тяжелых соматических заболеваний, частое и длительное лечение антибиотиками, проживание в домах престарелых. При высоком риске пенициллинорезистентности S. pneumoniae назначение макролидов может также оказываться неэффективным, поскольку возможно наличие перекрестной резистентности к макролидам. В то же время резистентность S. pneumoniae к пенициллину и макролидам не коррелирует с резистентностью к респираторным фторхинолонам, что делает рациональным и обоснованным выбор в подобных ситуациях респираторных фторхинолонов (левофлоксацин, моксифлоксацин). Другой проблемой антибиотикорезистентности является продукция H. influenzae b-лактамазы, что обычно наблюдается у больных ХОБЛ, часто получающих АП по поводу частых обострений заболевания. С учетом этого при развитии пневмонии на фоне ХОБЛ оправдано назначение защищенных пенициллинов (амоксициллин/клавуланат, ампициллин/сульбактам). Последние неэффективны в отношении пенициллинорезистентного S. pneumoniae, поскольку механизмы резистентности к пенициллину у S. pneumoniae и H. influenzae различны (снижение сродства пенициллин-связывающих белков). В то же время «защищенные» пенициллины могут сохранять активность по отношению к пенициллинорезистентным стафилококкам, вырабатывающим бета-лактамазу. Поэтому в ситуациях с высокой вероятностью стафилококковой внебольничной пневмонии (после перенесенного гриппа, хроническая алкогольная интоксикация) обосновано назначение ингибитор-защищенных пенициллинов. Нерационально назначение в качестве первоначального АП при внебольничной пневмонии ко-тримоксазола или тетрациклина в связи с высоким уровнем резистентности к этим АП основных возбудителей пневмонии.
Ситуации, не требующие продолжения АТ или смены АП
— cубфебрильная температура,
— сохранение сухого кашля,
— наличие крепитирующих хрипов,
— сохранение инфильтрации при отчетливой положительной динамике по данным рентгенологического исследования,
— увеличение СОЭ (при нормализации количества лейкоцитов и формулы крови).
Источник


