Ожог химия уксус вещество одним словом

23 января 201914106 тыс.
Любой химический ожог, как собственно и термальный, характеризуется повреждением тела человека при контакте с химическими веществами, способными вызвать разрушение тканей.
Это в большинстве случаев кислота, щелочь, летучие масла, битум, керосин и бензин, фосфор и т.д. Причем чаще всего пораженные участки относятся к верхним конечностям, реже к нижним, еще реже к туловищу. Но иногда от такого ожога страдают глаза, лицо или органы пищевода и полость рта.
Надо учитывать, что последствия такого ожога зависят от глубины, тяжести проникновения и концентрации химического вещества, а также от качества своевременно оказанного лечения. В этом материале мы рассмотрим виды химических ожогов, их фото, а также узнаем, какую первую помощь следует оказать человеку в домашних условиях при химическом ожоге кожи.
Степени химических ожогов
При таких ожогах чаще всего поражается кожа лица, кисти рук, пищевод и желудок. Основными веществами, вызывающими ожоги, являются кислоты (серная, соляная, азотная, плавиковая и др.), щёлочи (едкий натр, едкое кали и др.), бензин, керосин, соли тяжёлых металлов (хлористый цинк, азотнокислое серебро и др.), некоторые летучие масла, фосфор, битум.
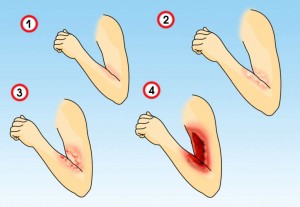
Тяжесть поражения кожи и слизистых оболочек при химическом ожоге зависит от концентрации вещества и длительности его действия на ткани. Всего принято выделять 4 степени тяжести ожога химическими веществами:
- 4 степень. Поражение затрагивает все ткани, включая кожный покров, мышцы и сухожилия.
- 3 степень. Поражению подвергаются те слои кожного покрова, которые расположены вблизи жировой подкожной ткани. Характерные особенности, свойственные ожогу этой степени, заключаются в появлении пузырей с жидкостью мутноватого оттенка или с примесью крови. В области поражения нарушается чувствительность, то есть, пострадавший не чувствует боли в рамках него.
- 2 степень. В этом случае поражение затрагивает, помимо верхнего слоя кожного покрова, еще и более глубокие его слои. Характеризуется ожог данной степени проявлениями в виде отечности и покраснения, кроме того, появляются также заполненные жидкостью прозрачного цвета пузырьки.
- 1 степень. Поражению подвергается только верхний слой кожного покрова. В числе основных проявлений, которые сопутствуют данному виду ожога, выделяют незначительный в выраженности отек и покраснение кожи. Помимо этого также в области поражения возникают легкие болезненные ощущения.
Примечательно, что признаки химического ожога в полной мере проявляются не сразу, потому оценить их степень можно лишь после оказания первой помощи. Первый симптом – жгучая боль на месте, куда попал химикат, и легкое покраснение. Если сразу же не начать оказывать помощь, ожог перейдет из 1 степени во 2 и даже 3, так как вещество продолжает действовать, проникая все глубже в слои ткани.
Первая помощь при химических ожогах
В домашних условиях оказание первой помощи при химических ожогах кожи включает: скорейшее удаление химического вещества с пораженной поверхности, снижение концентрации его остатков на коже за счет обильного промывания водой в течение 15-30 минут, охлаждение пораженных участков с целью уменьшения боли.
- При химических ожогах кислотой для нейтрализации используют 2-3% раствор питьевой соды.
- При ожогах щелочами – 1-2% раствор лимонной, борной или уксусной кислоты.
- При ожогах известью сначала сухим путём удаляют остатки извести и только потом длительно и энергично смывают поражённый участок.
- При ожогах фосфором необходимо сбросить горящую одежду или накинуть на горящую поверхность любую ткань, смоченную водой. Тушат пламя фосфора струёй воды из-под крана или 1-2% раствором медного купороса. Пинцетом удаляют все видимые частицы фосфора, после чего на обожжённую поверхность накладывают повязку, обильно смоченную 2% раствором медного купороса, 5% раствором двууглекислой соды или 3-5% раствором марганцевокислого калия.
Затем можно наложить стерильную повязку из марли, но не из ваты – ее использовать нельзя. В процессе нейтрализации химического агента с пострадавшего аккуратно снимается одежда, контактирующая с обожжённой областью, часы и украшения. Для снижения воспалительного процесса пострадавший участок кожи промывается прохладной водой, а пострадавшему необходимо дать сильный анальгетик (боль бывает вплоть до потери сознания).
При химическом ожоге обратитесь за неотложной медицинской помощью, если:
- У пострадавшего имеются признаки шока (потеря сознания, бледность, поверхностное дыхание).
- Пострадавший чувствует сильную боль, которую не удается снять с помощью безрецептурных анальгетиков, например, ацетаминофена или ибупрофена .
- Химический ожог распространился глубже первого слоя кожи и охватывает участок диаметром более 7,5 см.
- Затронуты глаза, руки, ноги, лицо, область паха, ягодиц или крупного сустава, а также полость рта и пищевод (если пострадавший выпил химическое вещество).
Отправляясь в отделение скорой помощи, возьмите с собой емкость с химическим веществом или его подробное описание для идентификации. Известная природа химического вещества дает возможность при оказании помощи в стационаре произвести его нейтрализацию, которую обычно трудно произвести в бытовых условиях.
Химический ожог пищевода
Может случиться так, что химическое вещество попало в пищевод и желудок. Это может быть сделано преднамеренно или оказаться несчастным случаем. Очень часто такими веществами оказываются аккумуляторный электролит и уксусная эссенция.
Более редкими случаями является попадание в пищевод и желудок щелочей или концентрированных кислот. У пострадавшего появляются сильные боли во рту, глотке, пищеводе, гортани и желудке. При поражении гортани больной может ощущать нехватку воздуха. Появляется рвота с кровавой слизью и кусочками слизистой желудка, которая отделяется из-за ожога.
Так как данного рода ожоги распространяются очень быстро, больной нуждается в оказании немедленной первой помощи, предусматривающей в самую первую очередь промывание желудка. Его можно промыть раствором питьевой соды, если речь идет об ожоге кислотами, либо слабым раствором уксусной кислоты при ожоге щелочами. В данном случае человеку нужно давать пить не просто большое, а действительно огромное количество жидкости, что даст возможность полностью избавиться от химического компонента.
При таких ожогах следует как можно быстрее вызвать врачей скорой помощи либо самостоятельно отвести больного в больницу.
Химический ожог глаза
Химический ожог глаза всегда считается тяжелой ситуацией с точки зрения лечения в офтальмологии. Все зависит от степени поражения, от агента, от глубины проникновения. Такой ожог может иногда привести не просто к ослаблению зрения, а даже к полной его потере.
- Химический ожог глаза кислотой самый «легкий» в лечении по сравнению с другими видами агентов.
- Химический ожог глаза щелочью сложен в лечении тем, что вызывает гидролиз самой структуры белка, что разрушает клетки и может быстро привести к влажному некрозу. Это способно затронуть внутриглазную жидкость и значительно повысить внутриглазное давление.
При химическом ожоге глаза в качестве первой помощи необходимо сделать обильное промывание и срочно обращаться к специалисту, лучше вызывать Скорую помощь.
Термический ожог кожи
Термические ожоги возникают вследствие воздействия огня, пара, горячей воды (кипятка), солнечных лучей и т.п. Наиболее часто термические ожоги получают от огня, они составляют 84 на 1000 пострадавших. Второе место занимают термические ожоги, полученные от горячих жидкостей, третье место – электроожоги.
Такие ожоги бывают трех степеней:
- I степень – покраснение кожных покровов, отек кожи;
- II степень – появление на месте ожога пузырей, наполненных прозрачной жидкостью;
- III степень – термические ожоги третьей степени подразделяют на два вида: IIIА (дермальные, поражение верхних слоев кожи) и IIIБ (омертвение всех слоев кожи, когда образуется некротический струп).
Источник
| Уксусная кислота | ||
|---|---|---|
| Систематическое наименование | Этановая кислота | |
| Традиционные названия | Уксусная кислота | |
| Хим. формула | C2H4O2 | |
| Рац. формула | CH3COOH | |
| Состояние | Жидкость | |
| Молярная масса | 60,05 г/моль | |
| Плотность | 1,0492 г/см³ | |
| Поверхностное натяжение | 27,1 ± 0,01 мН/м[4], 24,61 ± 0,01 мН/м[4] и 22,13 ± 0,01 мН/м[4] | |
| Динамическая вязкость | 1,056 мПа·с[5], 0,786 мПа·с[5], 0,599 мПа·с[5] и 0,464 мПа·с[5] | |
| Энергия ионизации | 10,66 ± 0,01 эВ[1] | |
| Температура | ||
| • плавления | 16,75 °C | |
| • кипения | 118,1 °C | |
| • вспышки | 103 ± 1 °F[1] и 39 ± 6 °C[2] | |
| • самовоспламенения | 427 ± 1 °C[3] | |
| Пределы взрываемости | 4 ± 0,1 об.%[1] | |
| Критическая точка | 321,6 °C, 5,79 МПа | |
| Мол. теплоёмк. | 123,4 Дж/(моль·К) | |
| Энтальпия | ||
| • образования | −487 кДж/моль | |
| Давление пара | 11 ± 1 мм рт.ст.[1], 10 ± 1 кПа[6] и 100 ± 1 кПа[6] | |
| Константа диссоциации кислоты | 4,76 (Ka=1,75*10-5) | |
| Показатель преломления | 1,372 | |
| Дипольный момент | 1,74 Д | |
| Рег. номер CAS | 64-19-7 | |
| PubChem | 176 | |
| Рег. номер EINECS | 200-580-7 | |
| SMILES | CC(=O)O | |
| InChI | 1S/C2H4O2/c1-2(3)4/h1H3,(H,3,4) QTBSBXVTEAMEQO-UHFFFAOYSA-N | |
| Кодекс Алиментариус | E260 | |
| RTECS | AF1225000 | |
| ChEBI | 15366 | |
| Номер ООН | 2789 | |
| ChemSpider | 171 | |
| Пиктограммы ECB | ||
| NFPA 704 | 2 3 1 ACID | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | ||
| Медиафайлы на Викискладе | ||
У́ксусная кислота (эта́новая кислота) CH3COOH — органическое соединение, cлабая, предельная одноосно́вная карбоновая кислота. Соли и сложные эфиры уксусной кислоты называются ацетатами.
История[править | править код]
Уксус является продуктом брожения вина и известен человеку с давних времен.
Первое упоминание о практическом применении уксусной кислоты относится к III веку до н. э. Греческий учёный Теофраст впервые описал действие уксуса на металлы, приводящее к образованию некоторых используемых в искусстве пигментов. Уксус применялся для получения свинцовых белил, а также ярь-медянки (зелёной смеси солей меди, содержащей помимо всего ацетат меди).
В Древнем Риме готовили специально прокисшее вино в свинцовых горшках. В результате получался очень сладкий напиток, который называли «сапа». Сапа содержала большое количество ацетата свинца — очень сладкого вещества, которое также называют свинцовым сахаром или сахаром Сатурна. Высокая популярность сапы была причиной хронического отравления свинцом, распространённого среди римской аристократии[7].
В VIII веке арабский алхимик Джабир ибн Хайян впервые изложил способы получения уксуса.
Во времена Эпохи Возрождения уксусную кислоту получали путём возгонки ацетатов некоторых металлов (чаще всего использовался ацетат меди (II)) (при сухой перегонке ацетатов металлов получается ацетон, вполне промышленный способ до середины XX века).
Свойства уксусной кислоты меняются в зависимости от содержания в ней воды. В связи с этим многие века химики ошибочно считали, что кислота из вина и кислота из ацетатов являются двумя разными веществами. Идентичность веществ, полученных различными способами, была показана немецким алхимиком XVI века Андреасом Либавиусом (нем. Andreas Libavius) и французским химиком Пьером Огюстом Аде (фр. Pierre Auguste Adet)[7].
Завод, производящий уксусную кислоту. 1884 год
В 1847 году немецкий химик Адольф Кольбе впервые синтезировал уксусную кислоту из неорганических материалов. Последовательность превращений включала в себя хлорирование сероуглерода до тетрахлорметана с последующим пиролизом до тетрахлорэтилена. Дальнейшее хлорирование в воде привело к трихлоруксусной кислоте, которая после электролитического восстановления превратилась в уксусную кислоту[8].
В конце XIX — начале XX века большую часть уксусной кислоты получали перегонкой древесины. Основным производителем уксусной кислоты являлась Германия. В 1910 году ею было произведено более 10 тысяч тонн кислоты, причем около 30 % этого количества было израсходовано на производство красителя индиго[7][9].
Физические свойства[править | править код]
Уксусная кислота представляет собой бесцветную жидкость с характерным резким запахом и кислым вкусом. Гигроскопична. Неограниченно растворима в воде. Смешивается со многими растворителями; в уксусной кислоте хорошо растворимы неорганические соединения и газы, такие как HF, HCl, HBr, HI и другие. Существует в виде циклических и линейных димеров[10].
Абсолютная уксусная кислота называется ледяной, так как при замерзании образует льдовидную массу. Способ получения ледяной уксусной кислоты в 1789 году открыл российский химик немецкого происхождения Товий Егорович Ловиц.
- Давление паров (в мм. рт. ст.):
- 10 (+17,1 °C)
- 40 (+42,4 °C)
- 100 (+62,2 °C)
- 400 (+98,1 °C)
- 560 (+109 °C)
- 1520 (+143,5 °C)
- 3800 (+180,3 °C)
- Относительная диэлектрическая проницаемость: 6,15 (+20 °C)
- Динамическая вязкость жидкостей и газов (в мПа·с): 1,155 (+25,2 °C); 0,79 (+50 °C)
- Поверхностное натяжение: 27,8 мН/м (+20 °C)
- Удельная теплоёмкость при постоянном давлении: 2,01 Дж/г·K (+17 °C)
- Стандартная энергия Гиббса образования ΔfG0 (298 К, кДж/моль): −392,5 (ж)
- Стандартная энтропия образования ΔfS0 (298 К, Дж/моль·K): 159,8 (ж)
- Энтальпия плавления ΔHпл: 11,53 кДж/моль
- Температура вспышки в воздухе: +38 °C
- Температура самовоспламенения на воздухе: 454 °C
- Теплота сгорания: 876,1 кДж/моль
Уксусная кислота образует двойные азеотропные смеси со следующими веществами.
| Вещество | tкип, °C | массовая доля уксусной кислоты |
|---|---|---|
| четырёххлористый углерод | 76,5 | 3 % |
| циклогексан | 81,8 | 6,3 % |
| бензол | 88,05 | 2 % |
| толуол | 104,9 | 34 % |
| гептан | 91,9 | 33 % |
| трихлорэтилен | 86,5 | 4 % |
| этилбензол | 114,65 | 66 % |
| о-ксилол | 116 | 76 % |
| п-ксилол | 115,25 | 72 % |
| бромоформ | 118 | 83 % |
- Уксусная кислота образует тройные азеотропные смеси
- с водой и бензолом (tкип +88 °C);
- с водой и бутилацетатом (tкип +89 °C).
Получение[править | править код]
В промышленности[править | править код]
Ранними промышленными методами получения уксусной кислоты были окисление ацетальдегида и бутана[11].
Ацетальдегид окислялся в присутствии ацетата марганца (II) при повышенной температуре и давлении. Выход уксусной кислоты составлял около 95 % при температуре +50—+60 °С.
Окисление н-бутана проводилось при 150 атм. Катализатором этого процесса являлся ацетат кобальта.
Оба метода базировались на окислении продуктов крекинга нефти. В результате повышения цен на нефть оба метода стали экономически невыгодными, и были вытеснены более совершенными каталитическими процессами карбонилирования метанола[11].
Каталитическое карбонилирование метанола[править | править код]
Каталитическая схема процесса фирмы Monsanto
Важным способом промышленного синтеза уксусной кислоты является каталитическое карбонилирование метанола моноксидом углерода[12], которое происходит по формальному уравнению:
Реакция карбонилирования метанола была открыта учеными фирмы BASF в 1913 году. В 1960 году эта компания запустила первый завод, производящий уксусную кислоту этим методом.[13] Катализатором превращения служил йодид кобальта. Метод заключался в барботаже монооксида углерода при температуре 180 °С и давлениях 200—700 атм через смесь реагентов. Выход уксусной кислоты составляет 90 % по метанолу и 70 % по СО. Одна из установок была построена в Гейсмаре (шт. Луизиана) и долго оставалась единственным процессом BASF в США[14].
Усовершенствованная реакция синтеза уксусной кислоты карбонилированием метанола была внедрена исследователями фирмы Monsanto в 1970 году.[15][16] Это гомогенный процесс, в котором используются соли родия в качестве катализаторов, а также йодид-ионы в качестве промоторов. Важной особенностью метода является большая скорость, а также высокая селективность (99 % по метанолу и 90 % по CO).[11]
Этим способом получают чуть более 50 % всей промышленной уксусной кислоты.[17]
В процессе фирмы BP в качестве катализаторов используются соединения иридия.
Биохимический способ производства[править | править код]
При биохимическом производстве уксусной кислоты используется способность некоторых микроорганизмов окислять этанол. Этот процесс называют уксуснокислым брожением. В качестве сырья используются этанолсодержащие жидкости (вино, забродившие соки), либо же просто водный раствор этилового спирта[18].
Реакция окисления этанола до уксусной кислоты протекает при участии фермента алкогольдегидрогеназы. Это сложный многоступенчатый процесс, который описывается формальным уравнением[19]:
Гидратация ацетилена в присутствии ртути и двухвалентных солей ртути[править | править код]
— Реакция Кучерова
Химические свойства[править | править код]
Уксусная кислота обладает всеми свойствами карбоновых кислот, и иногда рассматривается как их наиболее типичный представитель (в отличие от муравьиной кислоты, которая обладает некоторыми свойствами альдегидов). Связь между водородом и кислородом карбоксильной группы (−COOH) карбоновой кислоты является сильно полярной, вследствие чего эти соединения способны легко диссоциировать и проявляют кислотные свойства.
В результате диссоциации уксусной кислоты образуется ацетат-ион CH3COO− и протон H+. Уксусная кислота является слабой одноосновной кислотой со значением pKa в водном растворе равным 4,75. Раствор с концентрацией 1,0 M (приблизительная концентрация пищевого уксуса) имеет pH 2,4, что соответствует степени диссоциации 0,4 %.
На слабой диссоциации уксусной кислоты в водном растворе основана качественная реакция на наличие солей уксусной кислоты: к раствору добавляется сильная кислота (например, серная), если появляется запах уксусной кислоты, значит, соль уксусной кислоты в растворе присутствует (кислотные остатки уксусной кислоты, образовавшиеся из соли, связались с катионами водорода от сильной кислоты и получилось большое количество молекул уксусной кислоты)[20].
Исследования показывают, что в кристаллическом состоянии молекулы образуют димеры, связанные водородными связями[21].
Уксусная кислота способна взаимодействовать с активными металлами. При этом выделяется водород и образуются соли — ацетаты:
Уксусная кислота может хлорироваться действием газообразного хлора. При этом образуется хлоруксусная кислота:
Этим путём могут быть получены также дихлоруксусная (CHCl2COOH) и трихлоруксусная (CCl3COOH) кислоты.
Уксусная кислота может быть восстановлена до этанола действием алюмогидрида лития. Она также может быть превращена в хлорангидрид действием тионилхлорида. Натриевая соль уксусной кислоты декарбоксилируется при нагревании со щелочью, что приводит к образованию метана и карбоната натрия.
Уксусная кислота в биохимии организмов[править | править код]
Уксусная кислота образуется в живых организмах в процессе углеводного обмена, в том числе в организме человека в процессе биохимических реакции, в частности в цикле Кребса, утилизации алкоголя.
Применение[править | править код]
Уксусную кислоту, концентрация которой близка к 100 %, называют ледяной. 70—80%-й водный раствор уксусной кислоты называют уксусной эссенцией, а 3—15%-й — уксусом[22]. Водные растворы уксусной кислоты используются в пищевой промышленности (пищевая добавка E260) и бытовой кулинарии, а также в консервировании и для избавления от накипи. Однако количество уксусной кислоты, используемой в качестве уксуса, очень мало, по сравнению с количеством уксусной кислоты, используемой в крупнотоннажном химическом производстве.
Уксусную кислоту применяют для получения лекарственных и душистых веществ, таких как растворитель (например, в производстве ацетилцеллюлозы, ацетона). Она используется в книгопечатании и крашении.
Уксусная кислота используется как реакционная среда для проведения окисления различных органических веществ. В лабораторных условиях это, например, окисление органических сульфидов пероксидом водорода, в промышленности — окисление пара-ксилола кислородом воздуха в терефталевую кислоту.
Поскольку пары уксусной кислоты обладают резким раздражающим запахом, возможно её применение в медицинских целях в качестве замены нашатырного спирта для выведения больного из обморочного состояния (что является нежелательным, если только это необходимо для его эвакуации из опасного места его собственными силами).
Токсикология[править | править код]
Безводная уксусная кислота — едкое вещество. Пары уксусной кислоты раздражают слизистые оболочки верхних дыхательных путей. Предельно допустимая концентрация в атмосферном воздухе составляет 0,06 мг/м³, в воздухе рабочих помещений — 5 мг/м³[10][23]. Порог восприятия запаха уксусной кислоты в воздухе находится в районе 0,4 мг/л.[10] А по данным[24] порог восприятия запаха в группе (среднее значение) может достигать 300—500 мг/м3, что значительно превышает ПДК. Причём у отдельных людей он может быть значительно больше среднего значения.
Действие уксусной кислоты на биологические ткани зависит от степени её разбавления водой. Опасными считаются растворы, в которых концентрация кислоты превышает 30 %[10]. Концентрированная уксусная кислота способна вызывать химические ожоги, инициирующие развитие коагуляционных некрозов прилегающих тканей различной протяженности и глубины[25].
Токсикологические свойства уксусной кислоты не зависят от способа, которым она была получена[26]. Смертельная разовая доза составляет примерно 20 мл (при энтеральном приёме в перерасчёте на 100 % кислоту).
Последствиями приёма внутрь концентрированной уксусной кислоты являются тяжёлый ожог слизистой оболочки полости рта, глотки, пищевода и желудка; последствия всасывания уксусной эссенции — ацидоз, гемолиз, гемоглобинурия, нарушение свёртываемости крови, сопровождающееся тяжёлыми желудочно-кишечными кровотечениями. Характерно значительное сгущение крови из-за потери плазмы через обожжённую слизистую оболочку, что может вызвать шок. К опасным осложнениям отравления уксусной эссенцией относятся острая почечная недостаточность и токсическая дистрофия печени.
В качестве первой помощи при приёме уксусной кислоты внутрь следует выпить большое количество жидкости. Вызов рвоты является крайне опасным, так как вторичное прохождение кислоты по пищеводу усугубит ожог, также кислое содержимое может попасть в дыхательные пути. Допускается в целях нейтрализации кислоты и защиты слизистой приём жжёной магнезии, сырого яичного белка, киселя. Нельзя употреблять в этих целях соду, так как образующийся углекислый газ и вспенивание будет также способствовать забросу кислоты обратно в пищевод, гортань, а также может привести к прободению стенок желудка. Показано промывание желудка через зонд. Необходима немедленная госпитализация.
При ингаляционном отравлении парами требуется ополоснуть слизистые водой или 2 % раствором пищевой соды, приём внутрь молока, слабого щелочного раствора (2 % сода, щелочные минеральные воды) с последующей госпитализацией.
Примечания[править | править код]
- ↑ 1 2 3 4 https://www.cdc.gov/niosh/npg/npgd0002.html
- ↑ CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 16–19. — ISBN 978-1-4822-0868-9
- ↑ https://www.cdc.gov/niosh/ipcsneng/neng0363.html
- ↑ 1 2 3 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6–182. — ISBN 978-1-4822-0868-9
- ↑ 1 2 3 4 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6–232. — ISBN 978-1-4822-0868-9
- ↑ 1 2 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6–95. — ISBN 978-1-4822-0868-9
- ↑ 1 2 3 Martin, Geoffrey. Industrial and Manufacturing Chemistry (неопр.). — Part 1, Organic. — London: Crosby Lockwood, 1917. — С. 330—31.
- ↑ Goldwhite, Harold. Short summary of the career of the German organic chemist, Hermann Kolbe (англ.) // New Haven Section Bull. Am. Chem. Soc. : journal. — 2003. — September (vol. 20, no. 3).
- ↑ Schweppe, Helmut. Identification of dyes on old textiles (неопр.) // J. Am. Inst. Conservation. — 1979. — Т. 19, № 1/3. — С. 14—23. — doi:10.2307/3179569.
- ↑ 1 2 3 4 Уксусная кислота
- ↑ 1 2 3 Реутов О. А. Органическая химия. — М.: Изд-во МГУ, 1999. — Т. 4.
- ↑ Advances in Organometallic Chemistry
- ↑ Acetic Acid Production and Manufacturing Process
- ↑ Б. Лич. Катализ в промышленности. Том 1. — Москва: Мир, 1986. — 324 с.
- ↑ U.S. Patent 3 769 329
- ↑ Патент США
- ↑ Экологический фактор, или Окружающая среда как стимул эволюции промышленной химии
- ↑ Кандидат биологических наук Н. Кустова. Уксус. Что это такое и как его делают (недоступная ссылка). Интернет-ресурс «Всякая всячина». Дата обращения 2 сентября 2010. Архивировано 20 октября 2009 года.
- ↑ Биотехнология органических кислот и белковых препаратов: Учебное пособие (недоступная ссылка)
- ↑ Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. § 8. Реакции ионного обмена // Неорганическая химия. Учебник для 9 класса. — 7-е изд. — М.: Просвещение, 1976. — С. 15—18. — 2 350 000 экз.
- ↑ Jones, R.E.; Templeton, D.H. The crystal structure of acetic acid (англ.) // Acta Crystallogr. (англ.)русск. : journal. — International Union of Crystallography, 1958. — Vol. 11, no. 7. — P. 484—87. — doi:10.1107/S0365110X58001341.
- ↑ Уксус — статья из Большой советской энциклопедии.
- ↑ (Роспотребнадзор). № 2400. Этановая кислота (уксусная кислота) // ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны» (рус.) / утверждены А.Ю. Поповой. — Москва, 2018. — С. 162. — 170 с. — (Санитарные правила).
- ↑ Balavoine P. Observatiojns sur les Qualités Olfactifves et Gustatives des Aliments (англ.) // Mitteilungen aus dem Gebiete der Lebensmitteluntersuchung und Hygiene. — Bern: BAG, 1948. — Vol. 39. — P. 342–350. — ISSN 1424-1307. цитируется по: Odor Threshold Values p. 73.
- ↑ Уксусная кислота : Медицинский портал Eurolab
- ↑ www.textra-vita.com/technology Глава 17. Уксусная кислота 7. Токсиколого-гигиеническая оценка (недоступная ссылка). Дата обращения 16 мая 2011. Архивировано 25 мая 2012 года.
Ссылки[править | править код]
- Уксусная кислота
- Свойства
- Плотность водных растворов уксусной кислоты в зависимости от концентрации
Источник