Патогенез внебольничной пневмонии у детей
В статье представлены результаты исследования этиологии острых внебольничных пневмоний и острых бронхитов у детей в условиях стационара
Введение
Острые внебольничные пневмонии (ОВП) на сегодняшний день сохраняют свою значимость для клинической практики. Несмотря на то, что, по данным Государственного доклада «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2017 году», заболеваемость ОВП в 2017 г. составила 412,32 на 100 тыс. населения, что на 1,4% ниже, чем в предыдущем году (418,02), по среднемноголетнему показателю (СМП) заболеваемости ОВП в 2017 г. отмечался ее рост на 19,5% (заболеваемость на 100 тыс. населения в 2017 г. составила 412,32, а СМП (2011–2016 гг.) — 358,98) [1].
В течение последних 7 лет доля детей в общей структуре ОВП составляет чуть больше 30% (минимально — 32,3% в 2016 г., максимально — 35,8% в 2014 г). По данным Роспотребнадзора, с 2011 по 2017 г. в нашей стране ежегодная динамика числа установленных случаев ВП у детей до 17 лет и показателя заболеваемости на 100 тыс. населения носила волнообразный характер с тенденцией к увеличению данных показателей (рис. 1) [2].
В возрастной структуре ОВП у детей в 2017 г. отмечалось преобладание детей в возрасте от 1 до 6 лет
(рис. 2) [2].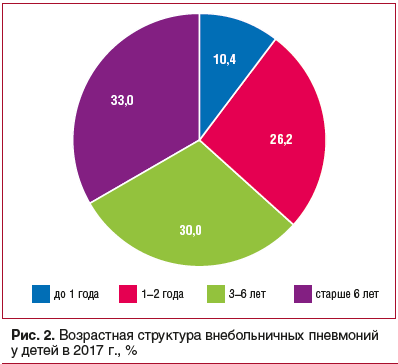
При этом, по данным Государственного доклада, в 2017 г. максимальный показатель заболеваемости ОВП наблюдался в возрастной группе 1–2 года (1470,06 на 100 тыс. населения данной возрастной группы) [1].
По данным Роспотребнадзора, на долю вирусных пневмоний в 2017 г. приходилось 1,2% от всех случаев ОВП, бактериальных — 27,7%, а доля ОВП пневмококковой этиологии составила 1,5% [2]. При этом в Государственном докладе было подчеркнуто, что отмечается снижение заболеваемости вирусной пневмонией в 2017 г. в 2 раза по сравнению с предыдущим годом (6,8 на 100 тыс. населения в 2016 г. и 3,35 на 100 тыс. населения в 2017 г.) и сохранение показателя заболеваемости ОВП бактериальной этиологии практически без изменений (117,25 на 100 тыс. населения в 2017 г. и 112,4 на 100 тыс. населения в 2016 г.) [1].
В Государственном докладе «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2017 году» поднята проблема верификации этиологии ОВП в клинической практике: «Необходимо отметить плохую этиологическую расшифровку внебольничных пневмоний в лабораториях медицинских организаций. В соответствии с отчетными формами нерасшифрованными остаются более 50% всех зарегистрированных ОВП» [1]. Своевременное установление этиологии ОВП определяет терапевтическую тактику, что становится принципиально важным, например, при вспышечной заболеваемости. Так, по данным Роспотребнадзора, в 2017 г. в 76,9% очагов ОВП этиологическим агентом явилась Mycoplasma pneumoniaе [1].
В этой связи актуальной клинической необходимостью является мониторинг возбудителей ОВП у детей, что и послужило целью настоящего исследования.
Материал и методы
Исследование проводилось на базе ДНО (ПК) ГБУЗ МО «Мытищинская городская клиническая больница» с февраля 2014 г. по март 2017 г. Под наблюдением находились 786 детей в возрасте от 3 до 17 лет, из них 497 детей с диагнозом ОБ и 289 детей с диагнозом ОВП легкой и средней степени тяжести (табл. 1).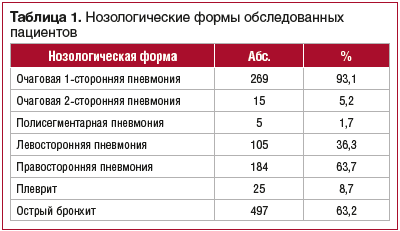
Установление этиологии ОБ и ОВП осуществлялось методом ПЦР (исследование мазков и/или отделяемого слизистой полости рта, носа, мокроты) (Центр молекулярной диагностики ФБУН ЦНИИ Эпидемиологии Роспотребнадзора); ИФА (с определением антител к следующим инфекциям: цитомегаловирусная (CMV), Эпштейна — Барр-
вирусная инфекция, герпесвирусы 1, 2, 6 типов, хламидийная, микоплазменная инфекции); микробиологическое исследование биологического материала из зева с определением чувствительности к антибактериальным препаратам (клинико-диагностическая лаборатория МБУЗ «МКГБ»).
Для верификации диагноза ОВП и при наличии показаний использовали инструментальные методы диагностики: рентгенографию грудной клетки, электрокардиографию (ЭКГ), исследование функции внешнего дыхания (ФВД), ультразвуковое исследование (УЗИ), которые проводились на базе ГБУЗ МО «МКГБ» в диагностическом отделении.
Статистическая обработка полученных данных осуществлялась на основании ГОСТ Р 50779.21–96 с использованием лицензионных программ (Microsoft Excel). Статистический анализ включал в себя анализ количественных и порядковых данных с расчетом значений среднего арифметического (M), стандартного отклонения (SD), ошибки среднего (m), медианы (Ме), 95% доверительного интервала (ДИ). Оценка качественных переменных проводилась путем расчета значений выборочной доли (W), ее стандартной ошибки (SE). Сравнение достоверности различий количественных и порядковых переменных между группами проводили после проверки допущений для применения параметрического многофакторного одномерного дисперсионного анализа с последующим расчетом достигнутых уровней значимости по t-критериям для связанных и несвязанных выборок или непараметрическим критериям. Различия считались достоверными при р<0,05, высокодостоверными — при p<0,01 и p<0,001, недостоверными — при р>0,05 [3].
Результаты исследования
В ходе исследования было установлено, что у более чем 60% пациентов с ОВП этиологическая структура носила сочетанный характер. Моноэтиологичные бактериальные ОВП были диагностированы у 22,7%, а доля моноэтиологичных вирусных пневмоний составила 4,5%, среди них вызванные вирусом парагриппа — 33%, RS-вирусом — 67% (рис. 3).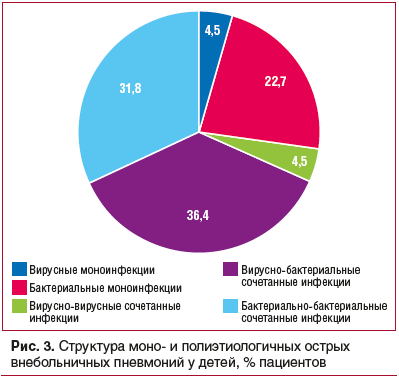
Среди бактериальных агентов наиболее часто при
ОВП у детей регистрировались Haemophilus influenzae, Mycoplasma pneumoniaе, Streptococcus pneumoniae. Обнаружение S. aureus у больных ОВП в мазках из носоглотки не свидетельствовало о значимости данного возбудителя как этиологического фактора ОВП и, наиболее вероятно, отражало носительство на слизистых верхних дыхательных путей. Среди вирусов при ОВП у детей наиболее часто определялись риновирус и вирус пара-
гриппа (рис. 4).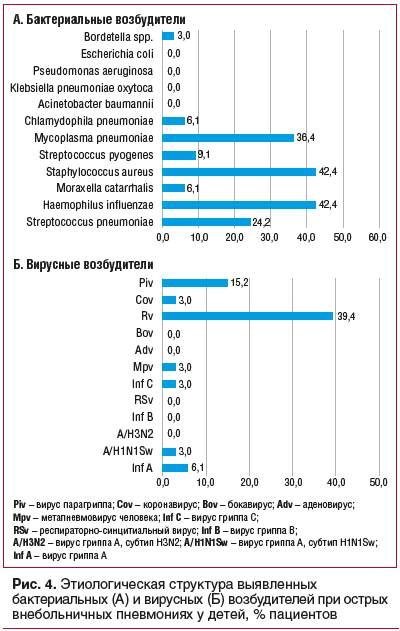
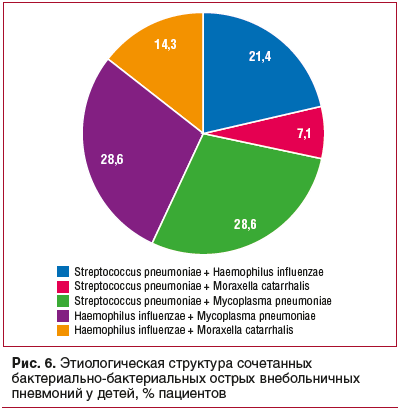
В этиологической структуре сочетанных вирусно-бактериальных ОВП у детей наиболее часто сочетанные инфекции были зарегистрированы при риновирусной инфекции, которая в 27,8% случаев сочеталась с пневмококковой инфекцией, в 11,1% — с Haemophilus influenzae, в 5,6% — с Mycoplasma pneumoniaе (рис. 5). Среди сочетанных форм бактериальных ОВП наиболее часто отмечались сочетания возбудителей Haemophilus influenzae, Mycoplasma pneumoniaе, Streptococcus pneumoniae (рис. 6).
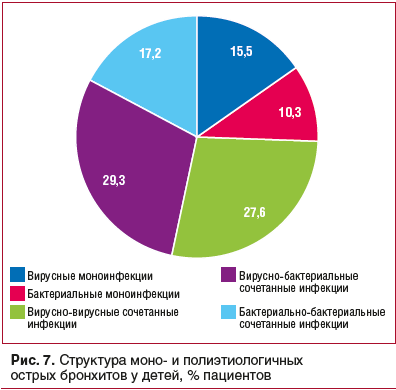
При ОБ у детей доля сочетанных форм инфекции составляла более 73%. При этом отмечались вирусно-вирусные, вирусно-бактериальные и бактериально-бактериальные сочетанные инфекции (рис. 7).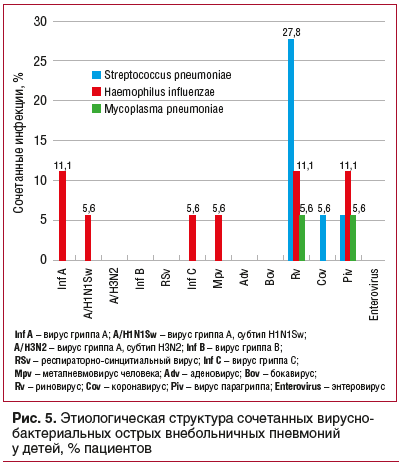

Наиболее частыми среди бактериальных агентов, выявленных у детей с ОБ, были Haemophilus influenzae, Moraxella catarrhalis, Streptococcus pneumoniae, а среди вирусов — риновирус и RS-вирус (рис. 8).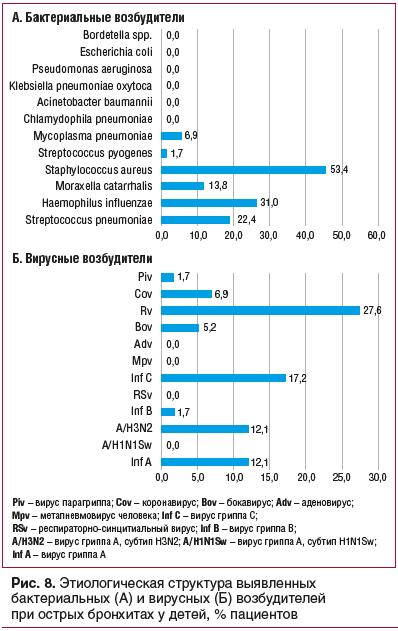
Сочетанные формы вирусно-бактериальных ОБ у детей наиболее часто отмечались при риновирусной инфекции, а наибольшая вариабельность сочетанных форм была отмечена при RS-вирусной инфекции
(рис. 9).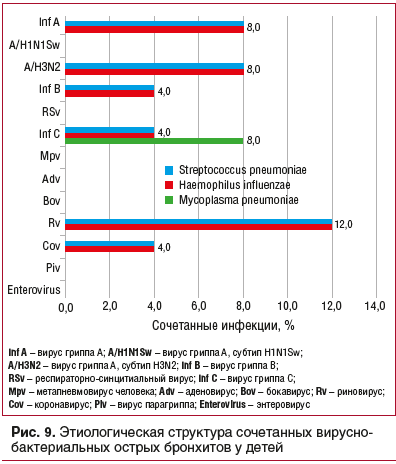
Наиболее часто среди сочетанных форм бактериально-бактериальных ОБ у детей были Haemophilus influenzae в сочетании с Moraxella catarrhalis или Streptococcus pneumoniae (рис. 10).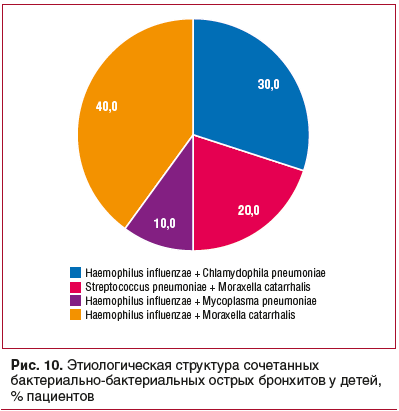
Сравнительный анализ сочетанных бактериальных форм ОВП и ОБ у детей показал, что при ОВП достоверно чаще регистрировались формы Mycoplasma pneumoniaе в сочетании с Haemophilus influenzae или Streptococcus pneumoniae, а также Haemophilus influenzae в сочетании с Chlamydophila pneumoniae. При ОП наиболее частой сочетанной формой была Haemophilus influenzae + Moraxella catarrhalis (рис. 11).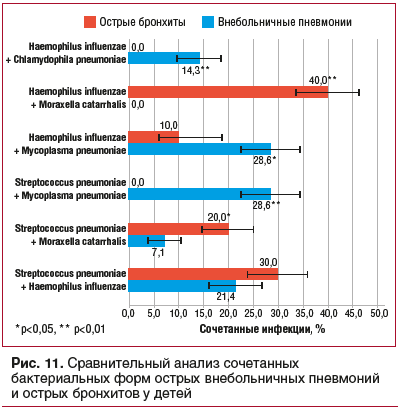
Расчет относительных рисков ОВП и ОБ у детей для различных возбудителей показал, что при ОВП они наиболее высокие при обнаружении Mycoplasma pneumoniaе и ее сочетанных форм, а при ОБ — при сочетанных формах Moraxella catarrhalis (табл. 2).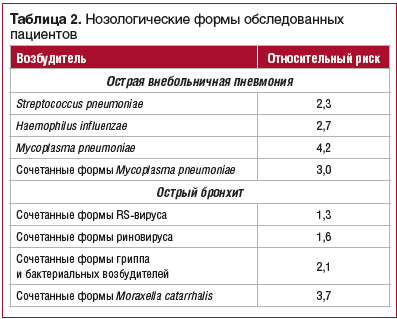
Заключение
Таким образом, установление этиологии ОВП и ОБ у детей является насущной проблемой клинической практики. Проведение мониторинга этиологической структуры позволило у большей части больных установить сочетанный характер ОВП и ОБ. Haemophilus influenzae и Streptococcus pneumoniae являются наиболее значимыми возбудителями как при моноинфекциях ОВП и ОБ у детей, так и в случае развития сочетанных форм. Отличительной особенностью ОВП у детей является высокая частота инфекций, обусловленных Mycoplasma pneumoniaе, в т. ч. в виде сочетанных инфекций, а при ОБ — Moraxella catarrhalis.
Источник
Пневмония у детей
Пневмония — острое инфекционное заболевание преимущественно бактериальной природы, характеризующееся очаговым поражением респираторных отделов лёгких, дыхательными расстройствами и вну- триальвеолярной экссудацией, а также инфильтра- тивными изменениями на рентгенограммах лёгких. Наличие рентгенологических признаков инфильтрации лёгочной паренхимы — «золотой стандарт» диагностики пневмонии, позволяющий отличать её от бронхита и бронхиолита.
Эпидемиология
Пневмонию диагностируют приблизительно у 20 из 1000 детей первого года жизни, приблизительно у 40 из 1000 в раннем и дошкольном возрасте, а в школьном и подростковом возрасте этот диагноз устанавливают приблизительно у 10 из 1000 детей.
Госпитальные пневмонии составляют от 6 до 27% всех случаев нозокомиальной инфекции, причём частота вентилятор-ассоциированных пневмоний превышает частоту обычных в 5—15 раз.
Смертность от этого заболевания остаётся довольно высокой даже в экономически развитых странах. В России смертность от внебольничной пневмонии достигает 13,1 на 100 000 населения. Чаще всего погибают дети раннего возраста (11,3 на 100 000 живорождённых).
Классификация
Пневмонии принято делить в зависимости от условий их возникновения на внебольничные (домашние) и больничные (госпитальные, нозокомиальные). Исключение составляют пневмонии новорождённых, которые делят на врождённые и приобретённые (постнатальные). Постнатальные пневмонии в свою очередь также могут быть внебольничными и больничными.
Под внебольничной пневмонией (ВП) понимают заболевание, развившееся в обычных условиях жизни ребёнка. Под госпитальной пневмонией (ГП) — заболевание, развившееся после трёхдневного пребывания ребёнка в стационаре или в течение первых 3 дней после его выписки.
Принято рассматривать вентилятор-ассоциированные госпитальные пневмонии (ВАГП) и вентилятор-неассоциированные госпитальные пневмонии (ВнАГП). Выделяют ВАГП ранние, развивающиеся в первые 3 сут искусственной вентиляции лёгких (ИВЛ), и поздние, развивающиеся начиная с 4-х сут ИВЛ.
Пневмония может поражать целую долю лёгкого (долевая пневмония), один или несколько сегментов (сегментарная или полисегментарная пневмония), альвеолы или группы альвеол (очаговая пневмония), прилежащие к бронхам (бронхопневмония), или затрагивать интерстициальную ткань (интерстициальная пневмония). Эти различия выявляются главным образом при физикальном и рентгенологическом обследовании.
По тяжести течения, степени поражения лёгочной паренхимы, наличию интоксикации и осложнений выделяют нетяжёлые и тяжёлые, неосложнённые и осложнённые пневмонии.
К осложнениям пневмонии относят инфекционно-токсический шок с развитием полиорганной недостаточности, деструкцию лёгочной паренхимы (буллы, абсцессы), вовлечение плевры в инфекционный процесс с развитием плеврита, эмпиемы или пневмоторакса, медиастинит и т.д.
Настоящая лекция посвящена внебольничной пневмонии у детей и подростков.
Этиология
Наиболее частые возбудители внебольничных пневмоний — Streptococcus pneumoniae (20—60%), Mycoplasma pneumoniae (5—50%), Chlamydia pneumoniae (5—15%), Chlamydia trachomatis (3—10%),
Haemophilus influenzae (3—10%), Enterobacteriaceae (Klebsiella pneumoniae, Escherichia coli и др. — 3—10%), Staphylococcus aureus (3—10%), Streptococcus pyogenes, Chlamydia psittaci, Coxiella burneti и др. Однако необходимо учитывать, что этиология пневмоний у детей и подростков весьма тесно связана с возрастом.
В первые 6 мес жизни ребёнка этиологическая роль пневмококка и гемофильной палочки незначительна, поскольку от матери внутриутробно передаются антитела к этим возбудителям. Ведущую роль в этом возрасте играют Е. coli, К pneumoniae и S. aureus. Этиологическая значимость каждого из них не превышает 10—15%, но именно они обусловливают наиболее тяжёлые формы заболевания, осложняющиеся развитием инфекционно- токсического шока и деструкции лёгких. Другая группа пневмоний этого возраста — пневмонии, вызванные атипичными возбудителями, в основном С. trachomatis, которыми дети заражаются от матери интранатально, редко — в первые дни жизни. Возможно также заражение P. carinii, что особенно значимо для недоношенных детей.
Начиная с 6 мес и до 6—7 лет пневмонии в основном вызывает S. pneumoniae (60%). Нередко высевают и бескапсульную гемо- фильную палочку. Н. influenzae типа b выявляют реже (7—10%), она обусловливает, как правило, тяжёлые пневмонии, осложнённые деструкцией лёгких и плевритом.
Пневмонии, вызванные S. aureus и S. pyogenis, выявляют в 2—3% случаев обычно в качестве осложнений тяжёлых вирусных инфекций, таких, как грипп, ветряная оспа, корь и герпес. Пневмонии, вызванные атипичными возбудителями у детей этого возраста, обусловлены в основном М. pneumoniae и С. pneumoniae. Надо сказать, что роль М. pneumoniae в последние годы явно возросла. Микоплазменную инфекцию в основном диагностируют на втором или третьем году жизни, а инфицирование С. pneumoniae — у детей старше 5 лет.
Вирусы у детей этой возрастной группы могут быть как самостоятельной причиной заболевания, так и участником вирусно-бактериальных ассоциаций. Наибольшее значение имеет респираторно-синтициальный (PC) вирус, который встречается приблизительно в половине случаев заболевания вирусной и вирусно-бактериальной природы. В четверти случаев этиологическим фактором становятся вирусы парагриппа типов 1 и 3. Вирусы гриппа А и В и аденовирусы играют небольшую роль. Редко выявляют риновирусы, энтеровирусы, коронавирусы. Описаны также пневмонии, обусловленные вирусами кори, краснухи и ветряной оспы. Как уже говорилось, помимо самостоятельной этиологической значимости, респираторно-вирусная инфекция у детей раннего и дошкольного возраста — практически обязательный фон для развития бактериального воспаления.
Этиология пневмонии у детей старше 7 лет и подростков практически не отличается от таковой у взрослых. Наиболее часто пневмонии вызывают S. pneumoniae (35—40%) и М. pneumoniae (23—44%), реже — С. pneumoniae (10—17%). Н. influenzae типа Ь, а такие возбудители, как Enterobacteriaceae (К. pneumoniae, Е. coli и др.) и S. aureus, практически не встречаются.
Особо стоит упомянуть о пневмонии у пациентов с иммунодефицитом. У детей с первичными клеточными иммунодефицитами, у ВИЧ-инфицированных пациентов и больных СПИДом пневмонию чаще вызывают Pneumocysticus carinii и грибы рода Candida, а также Л/, avium-intracellare и цитомегаловирус. При гуморальном иммунодефиците чаще высевают S. pneumoniae, а также стафилококки и энтеробактерии, при нейтропении — грамотрицательные энтеробактерии и грибы (табл. 14-1).
Таблица 14-1. Этиология внебольничных пневмоний у больных с иммунодефицитом
Группы больных | Патогены |
Больные с первичным клеточным иммунодефицитом | Пневмоцисты Грибы рода Candida |
Больные с первичным гуморальным иммунодефицитом | Пневмококки Стафилококки Энтеробактерии |
Больные с приобретённым иммунодефицитом (ВИЧ-инфицированные, больные СПИДом) | Пневмоцисты Цитомегаловирусы Микобактерии туберкулёза Грибы родаCandida |
Больные с нейтропенией | Грамотрицательные энтеробактерии Грибы родаCandida, Aspergillus, Fusarium |
Патогенез
Из особенностей патогенеза пневмонии у детей раннего возраста наиболее важен низкий уровень противоинфекционной защиты. Кроме того, можно отметить относительную недостаточность мукоцилиарного клиренса, особенно при респираторно-вирусной инфекции, с которой, как правило, и начинается пневмония у ребёнка. Склонность к отёку слизистой оболочки дыхательных путей и образованию вязкой мокроты также способствует нарушению мукоцилиарного клиренса.
Известны четыре основные причины развития пневмонии:
• аспирация секрета ротоглотки;
• вдыхание аэрозоля, содержащего микроорганизмы;
• гематогенное распространение микроорганизмов из внелёгоч- ного очага инфекции;
• непосредственное распространение инфекции из соседних поражённых органов.
У детей наибольшее значение имеет микроаспирация секрета ротоглотки. Аспирация большого количества содержимого верхних дыхательных путей и/или желудка характерна для новорождённых и детей первых месяцев жизни. Реже происходит аспирация во время кормления и/или при рвоте и срыгиваниях. У детей раннего и дошкольного возраста наиболее значима обструкция дыхательных путей, особенно в случае развития бронхообструктивного синдрома.
Факторы, предрасполагающие к аспирации/микроаспирации
• Энцефалопатия различного генеза (постгипоксическая, при пороках развития мозга и наследственных заболеваниях, судорожном синдроме).
• Дисфагия (синдром рвоты исрыгивания, пищеводно-трахеальные свищи, ахалазия кардии, гастроэзофагеальный рефлюкс).
• Бронхообструктивный синдром при респираторной, в том числе вирусной, инфекции.
• Механические нарушения защитных барьеров (назогастраль- ный зонд, интубация трахеи, трахеостомия, эзофагогастродуо- деноскопия).
• Повторная рвота при парезе кишечника, тяжёлых инфекционных и соматических заболеваниях.
Клиническая картина
Классические проявления пневмонии неспецифичны — это одышка, кашель (с мокротой и без неё), повышение температуры тела, слабость, симптомы интоксикации. Следует предполагать развитие пневмонии, если у ребёнка появляются кашель и/или одышка, особенно в сочетании с повышением температуры тела. Соответствующие перкуторные и аускультативные изменения в лёгких, а именно укорочение перкуторного звука, ослабление или, наоборот, появление бронхиального дыхания, крепитация или мелкопузырчатые хрипы определяют лишь в 50—77% случаев. Следует помнить, что в раннем детском возрасте, особенно у детей первых месяцев жизни, эти проявления типичны практически для любой острой респираторной инфекции, а физикальные изменения в лёгких при пневмонии в большинстве случаев (за исключением лобарных пневмоний) практически неотличимы от изменений при бронхите.
По данным ВОЗ, для пневмонии наиболее характерны:
• лихорадочное состояние с температурой тела выше 38 °С в течение 3 сут и более;
• одышка (с числом дыхательных движений более 60 в минуту для детей до 3 мес, более 50 в минуту — до 1 года, более 40 в минуту — до 5 лет);
• втяжение уступчивых мест грудной клетки.
Осложнения
Внутрилёгочные деструкции
Внутрилёгочные деструкции представляют собой нагноение с образованием булл или абсцессов на месте клеточной инфильтрации в лёгких, вызываемых некоторыми серотипами пневмококка, стафилококками, Я. influenzae типа Ь, гемолитическим стрептококком, клебсиеллой, синегнойной палочкой. Лёгочные нагноения сопровождаются лихорадкой и нейтрофильным лейкоцитозом до момента опорожнения, которое происходит либо в бронх, сопровождаясь усилением кашля, либо в полость плевры, вызывая пиопневмоторакс.
Синпневмонический плеврит
Синпневмонический плеврит могут вызывать любые бактерии и вирусы, начиная с пневмококка и завершая микоплазмой и аденовирусом. Для гнойного экссудата характерен низкий рН (7,0—7,3), цитоз выше 5000 лейкоцитов в 1 мкл. Кроме того, экссудат может быть фибринозно-гнойным или геморрагическим. При адекватной антибактериальной терапии экссудат теряет гнойный характер и плеврит постепенно разрешается. Однако полное выздоровление происходит через 3—4 нед.
Метапневмонический плеврит
Метапневмонический плеврит обычно развивается в стадии разрешения пневмококковой, реже — гемофильной пневмонии. Основная роль в его развитии принадлежит иммунологическим процессам, в частности образованию иммунных комплексов в полости плевры на фоне распада микробных клеток.
Как уже говорилось, метапневмонический плеврит развивается в стадии разрешения пневмонии через 1—2 дня нормальной или субнормальной температуры. Температура тела вновь повышается до 39,5—40,0 °С, выражено нарушение общего состояния. Лихорадочный период продолжается в среднем 7 дней, причём антибактериальная терапия не оказывает на него влияния. Рентгенологически обнаруживают плеврит с хлопьями фибрина, у части детей при эхокардиографии выявляют перикадит. В анализе периферической крови число лейкоцитов нормальное или сниженное, а СОЭ увеличена до 50—60 мм/ч. Рассасывание фибрина происходит медленно, в течение 6—8 нед, из-за низкой фибрино- литической активности крови.
Пиопневмоторакс
Пиопневмоторакс развивается в результате прорыва абсцесса или буллы в полость плевры. Происходит увеличение количества воздуха в плевральной полости и, как следствие, смещение средостения.
Пиопневмоторакс обычно развивается неожиданно: остро возникают болевой синдром, нарушения дыхания вплоть до дыхательной недостаточности. При напряжённом клапанном пиопнев- мотораксе показана срочная декомпрессия.
Диагностика пневмонии у детей
• При физикальном обследовании особое внимание обращают на выявление следующих признаков:
§ укорочение (притупление) перкуторного звука над поражённым участком лёгкого;
§ локальное бронхиальное дыхание, звучные мелкопузырчатые
хрипы или инспираторную крепитацию при аускультации;
§ усиление бронхофонии и голосового дрожания у детей старшего возраста.
В большинстве случаев выраженность этих симптомов зависит от многих факторов, включая тяжесть заболевания, распространённость процесса, возраст ребёнка, наличие сопутствующих заболеваний. Необходимо помнить, что физикальные симптомы и кашель могут отсутствовать примерно у 15—20% пациентов.
Анализ периферической крови необходимо проводить всем пациентам с подозрением на пневмонию. Количество лейкоцитов около 10—12х109/л указывает на высокую вероятность бактериальной инфекции. Лейкопения менее Зх109/л или лейкоцитоз более 25×109/л — неблагоприятные прогностические признаки.
Рентгенография органов грудной клетки является основным методом диагностики пневмонии. Главный диагностический признак — воспалительный инфильтрат. Кроме того, оценивают следующие критерии, которые свидетельствуют о тяжести заболевания и помогают в выборе антибактериальной терапии:
• инфильтрацию лёгких и её распространённость;
• наличие или отсутствие плеврального выпота;
• наличие или отсутствие деструкции лёгочной паренхимы. Повторная рентгенография позволяет оценить динамику процесса на фоне проводимого лечения и полноту выздоровления.
Таким образом, клинико-рентгенологическими критериями диагноза внебольничной пневмонии считают наличие изменений в лёгких инфильтративного характера, выявленных при рентгенографии органов грудной клетки, в сочетании хотя бы с двумя из перечисленных ниже клинических признаков:
• острое лихорадочное начало заболевания (Т >38,0 °С);
• кашель;
• аускультативные признаки пневмонии;
• лейкоцитоз >10х109/л и/или палочкоядерный сдвиг >10%. Важно помнить, что клинико-рентгенологический диагноз не может быть приравнен к этиологическому диагнозу!
Биохимический анализ крови — стандартный метод обследования детей с тяжёлыми пневмониями, нуждающихся в госпитализации. Определяют активность печёночных ферментов, уровень креатинина и мочевины, электролитов в крови. Кроме того, определяют кислотно-основное состояние крови. У детей раннего возраста проводят пульсоксиметрию.
Посев крови выполняют только при тяжёлой пневмонии и, по возможности, до применения антибиотиков с целью постановки этиологического диагноза.
Микробиологическое исследование мокроты в педиатрии не имеет широкого применения в связи с техническими трудностями забора мокроты у детей младше 7—10 лет. Его проводят главным образом при бронхоскопии. В качестве материала для исследования берут откашливаемую мокроту, аспираты из носоглотки, трахеостомы и эндотрахеальной трубки, посевы пунктата плеврального содержимого.
Серологические методы исследования также используют с целью выяснения этиологии заболевания. Нарастание титров специфических антител в парных сыворотках, взятых в острый период и в период выздоровления, может свидетельствовать о микоплазменной, хламидийной или легионеллёзной инфекции. Этот метод, однако, не влияет на тактику лечения и имеет только эпидемиологическую значимость.
Компьютерная томография обладает в 2 раза более высокой чувствительностью при выявлении очагов инфильтрации в нижней и верхней долях лёгких. Используют её при проведении дифференциальной диагностики.
Фибробронхоскопия и другие инвазивные методики применяют с целью получения материала для микробиологического исследования у пациентов с тяжёлыми нарушениями иммунитета и при проведении дифференциальной диагностики.
Дифференциальный диагноз
Дифференциальный диагноз пневмоний у детей тесно связан с возрастом ребёнка, так как определяется особенностями лёгочной патологии в различные возрастные периоды.
В грудном возрасте необходимость в проведении дифференциальной диагностики возникает при заболеваниях, трудно поддающихся стандартному лечению. В этих случаях следует помнить, что, во-первых, пневмония может осложнять другую патологию, во-вторых, клинические проявления дыхательной недостаточности могут быть обусловлены другими состояниями:
• аспирацей;
• инородным телом в бронхах;
• не диагностированной ранее трахеоэзофагеальной фистулой, гастроэзофагеальным рефлюксом;
• пороками развития лёгкого (долевая эмфизема, колобома), сердца и крупных сосудов;
• муковисцидозом и дефицитом агантитрипсина.
У детей 2—3 лет жизни и в более старшем возрасте следует исключить:
• синдром Картагенера;
• гемосидероз лёгких;
• неспецифический альвеолит;
• селективный иммунодефицит IgA.
Диагностический поиск у пациентов этого возраста основывается на эндоскопическом исследовании трахеи и бронхов, проведении сцинтиграфии и ангиографии лёгких, проб на муковисцидоз, определении концентрации агантитрипсина и др. Наконец, во всех возрастных группах необходимо исключить туберкулёз лёгких.
У пациентов с тяжёлыми дефектами иммунитета при появлении одышки и очагово-инфильтративных изменений в лёгких необходимо исключить:
• прогрессирование основного заболевания;
• вовлечение лёгких в основной патологический процесс (например, при системных заболеваниях соединительной ткани);
• последствия проводимой терапии (лекарственное поражение лёгких, лучевой пневмонит).
Источник


