Рациональная антибактериальная терапия при пневмонии
СОДЕРЖАНИЕ
ОБЩИЕ СВЕДЕНИЯ
ВАЖНО ЗНАТЬ
ТАКТИКА И СТРАТЕГИЯ ЛЕЧЕНИЯ ПНЕВМОНИИ У ВЗРОСЛЫХ
ЛЕЧЕНИЕ ПНЕВМОНИИ В СТАЦИОНАРЕ
ЗАКЛЮЧЕНИЕ
Внебольничная пневмония (синонимы: домашняя пневмония, амбулаторная, воспаление легких) — это острое инфекционное заболевание легких, возникшее во внебольничных условиях или в первые 48 часов госпитализации, сопровождающееся симптомами инфекции нижних дыхательных путей (температура, кашель, боли в груди, одышка) и «свежими» очагово-инфильтративными изменениями в легких при отсутствии очевидной диагностической альтернативы. Внебольничная пневмония у взрослых (воспаление легких у взрослых) довольно распространена. По результатам современных эпидемиологических исследований, заболеваемость внебольничной пневмонией у взрослых составляет 3-40%, около 50% из них госпитализируются. При этом каждый 10-й пациент с внебольничной пневмонией в силу тяжелого или осложненного течения заболевания помещается в отделение интенсивной терапии (ОИТ). И если летальность среди амбулаторных больных, как правило, не превышает 0,5 %, то госпитальная летальность достигает 14 % и более.
Согласно данным официальной статистики, заболеваемость пневмонией в РФ в 2018 г. составила 490,6 на 100 тыс., что на 19 % превысило аналогичный показатель, зарегистрированный в 2017 г. (412,3/100 000); отмечен также и рост летальности (на 2,2 %) больных внебольничной пневмонией – с 19,11/100 000 в 2017 г. до 19,8/100 000 в 2018 г.
При этом ведущее место в достижении оптимального исхода у данной категории пациентов занимает своевременно начатая рациональная антибактериальная терапия (АБТ).
Основные вопросы, связанные с антибактериальной терапией (антибиотики при пневмонии):
I. Стратификация пациентов. При выборе антибиотика нужно учитывать факторы риска неблагоприятного исхода и степень тяжести заболевания. Также следует принять во внимание наличие известных факторов риска появления отдельных возбудителей внебольничной пневмонии у взрослых – лекарственноустойчивых Streptococcus pneumoniae 1*, грамотрицательных энтеробактерий *2, Pseudomonas aeruginosa *3.
1*Возраст > 65 лет, терапия β-лактамами в течение последних 3 мес, множественные сопутствующие заболевания внутренних органов (сахарный диабет, сердечная недостаточность, ХОБЛ и др.) и др.
2*Обитатели домов престарелых, проводимая антибактериальная терапия, множественные сопутствующие заболевания и др.
3*«Структурные» заболевания легких (например, бронхоэктазия), системная терапия глюкокортикоидами, упадок питания, терапия антибиотиками широкого спектра действия более 7 дней в течение последнего месяца.
II. Соотношение «цена/эффективность». Идеальный антибиотик – это не самый дешевый препарат. Оценивая прямые затраты на лечение (прежде всего, в амбулаторных условиях), со стоимостью лекарственного средства нужно соотнести длительность нетрудоспособности пациента и частоту терапевтических неудач, в том числе повлекших за собой госпитализацию. Разумеется, что стоимость антибактериальной терапии зачастую несопоставима с последствиями терапевтической неудачи.
III. Приверженность пациента лечебным рекомендациям. Серьезными препятствиями к выполнению пациентом назначений являются: обилие и частота приема лекарственных препаратов, влияние лечения на сложившийся жизненный стереотип и минимальные последствия несоблюдения врачебных рекомендаций в представлении больного.
При решении этих и других вопросов, связанных с антибактериальной терапией, нужно учитывать следующее:
а) традиционные диагностические тесты, направленные на этиологическую верификацию ВП, характеризуются ограниченной ценностью (их результативность не превышает 50 %);
б) антибактериальная терапия пневмонии, по крайней мере в дебюте заболевания, носит эмпирический характер;
в) выбор и время начала АБТ имеют определяющее прогностическое значение;
г) ключевыми возбудителями большинства случаев внебольничной пневмонии являются Streptococcus pneumoniae (пневмококк), Haemophilus influenzae, «атипичные» микроорганизмы (Chlamydophila pneumoniae, Mycoplasma pneumoniae);
д) доказан реальный вклад коинфекции (например, сочетании пневмококка и «атипичных» возбудителей) в развитие внебольничной пневмонии;
е) все более актуальной становится проблема распространения лекарственноустойчивых штаммов основных возбудителей внебольничной пневмонии.
В целом же выбор обоснованной эмпирической антибактериальной терапии внебольничной пневмонии строится на знании ограниченного перечня возбудителей заболевания и предсказуемых уровней резистентности в пределах обширных географических регионов. Так, к числу основных возбудителей внебольничной пневмонией нетяжелого течения, т. е. не требующей госпитализации, относятся S. pneumoniae, M. pneumoniae, C. pneumoniae, тогда как среди микробиологических «находок» у больных с более тяжелым течением заболевания, нуждающихся в госпитализации (в т. ч. в ОИТ), наряду с пневмококком, H. influenzae фигурируют Legionella pneumophila, представители семейства Enterobacteriaceae (прежде всего, Klebsiella pneumoniae, Escherichia coli), Staphylococcus aureus.
В выборе рациональной антибактериальной терапии, помимо ориентированности в этиологии ВП, не менее важно знать структуру лекарственной устойчивости ключевых возбудителей заболевания, и, прежде всего, пневмококка. В некоторых странах устойчивость пневмококков к пенициллину достигает 60 %, причем многие из них обладают резистентностью к трем и более классам антибиотиков. Резистентность S. pneumoniae к пенициллину обычно сочетается с устойчивостью к цефалоспоринам I–II поколений, тетрациклинам, ко-тримоксазолу.
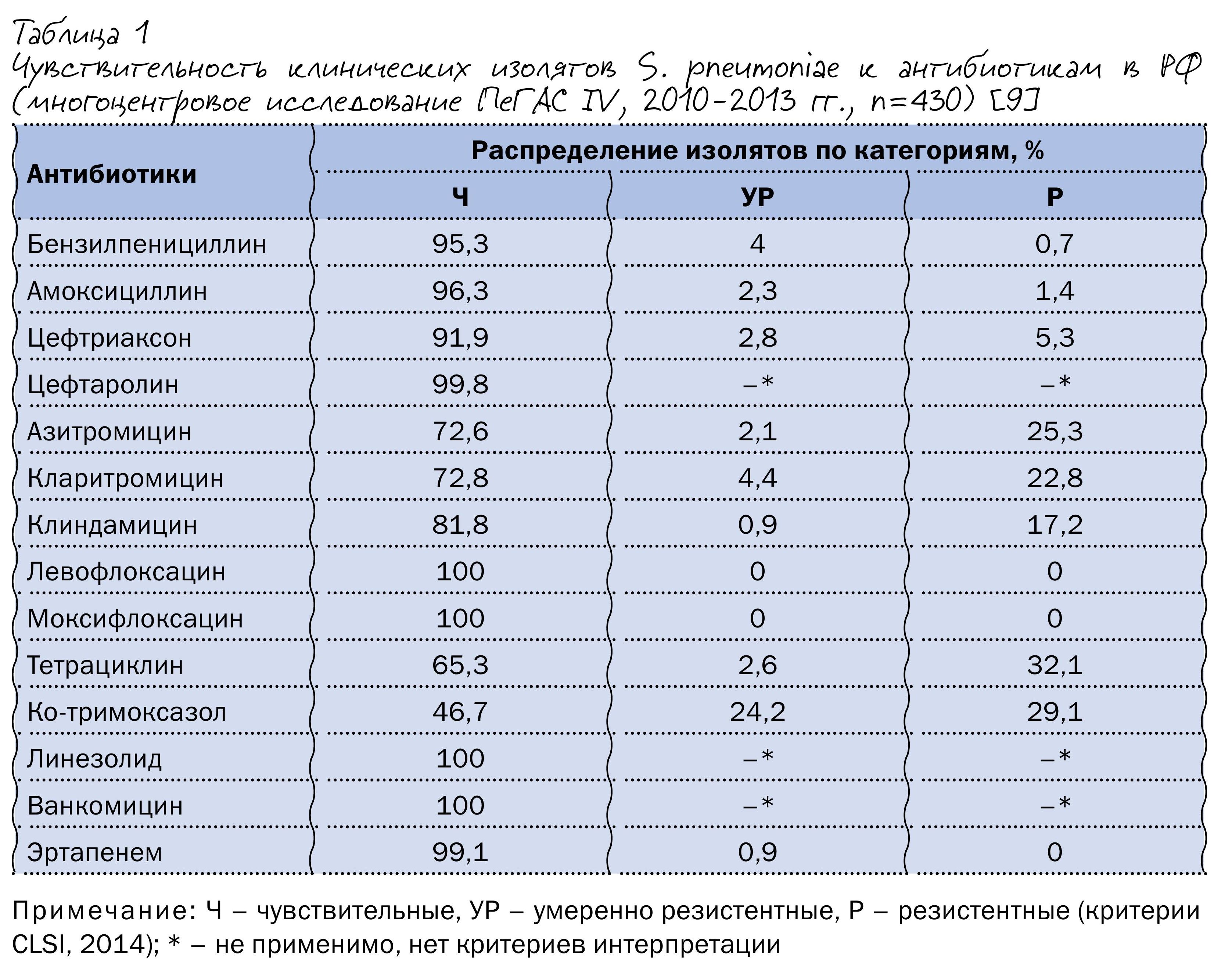
Данные мониторинга чувствительности клинических штаммов S. pneumoniae в РФ, выделенных у пациентов с внебольничными инфекциями нижних дыхательных путей в 2010–2013 гг., представлены в таблице 1. Отличительная черта нашей страны – высокий уровень резистентности пневмококка к тетрациклинам и ко-тримоксазолу, что может быть связано с неоправданно высокой частотой их применения в XX – начале XXI вв. Уровень же устойчивости S. pneumoniae к пенициллину и аминопенициллинам остается относительно невысоким – 4,7 и 1,4 % изолятов соответственно.
Резистентность пневмококка к различным макролидам и линкозамидам варьирует в пределах 18–27,4 %; большинство макролидорезистентных пневмококков демонстрируют устойчивость к клиндамицину, что может свидетельствовать о преобладании в РФ MLSB-фенотипа резистентности, обусловленного модификацией мишени и определяющего устойчивость S. pneumoniae ко всем макролидам, включая 16-членные.
В настоящее время появились доказательства превосходства некоторых подходов к лечению взрослых больных ВП. Так, целесообразность раннего назначения антибиотиков (в первые 4–8 ч от момента госпитализации) подтверждаются результатами обсервационных исследований и согласуется с мнением экспертов.
Для снижения затрат можно использовать современные рекомендации, облегчающие выбор пациентов ВП, которые могли бы безопасно и эффективно лечиться в амбулаторных условиях.
По возможности ранний переход с парентерального введения антибиотика на его прием внутрь и следующая за этим выписка из стационара (когда пациент становится клинически стабильным) также снижает стоимости лечения.
Выбор препаратов для стартовой антибактериальной терапии больных внебольничной пневмонией определяет спектр потенциальных возбудителей заболевания и профиль антибиотикорезистентности. При этом важно иметь в виду, что «…данные, полученные из существующих рандомизированных клинических исследований, не позволяют создать доказательные рекомендации по выбору антибиотика для терапии внебольничной пневмонии». Поэтому стратификация больных и рекомендации по выбору антибактериальной пневмонии в большей степени отражают национальные эпидемиологические данные антибиотикорезистентности ключевых возбудителей внебольничной пневмонии, их потенциальное экологическое влияние, а также учитывают затратную эффективность лекарственной терапии.
Согласно положениям проекта национальных рекомендаций, подготовленных экспертами Российского респираторного общества (РРО) и Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии (МАКМАХ), среди больных пневмонией, которые могут получать лечение в амбулаторных условиях, целесообразно выделять 2 группы. В первую из них включены пациенты без серьезных хронических заболеваний внутренних органов, не принимавшие за последние 3 мес системные антибиотики и не имеющие другие факторы риска инфицирования редкими и/или полирезистентными возбудителями (пребывание в доме престарелых или других учреждениях длительного ухода, наличие госпитализаций по любому поводу в течение ≥2 суток в предшествующие 90 дней, в/в инфузионная терапия, лечение ран в домашних условиях в предшествующие 30 дней и др.) (рис. 1).
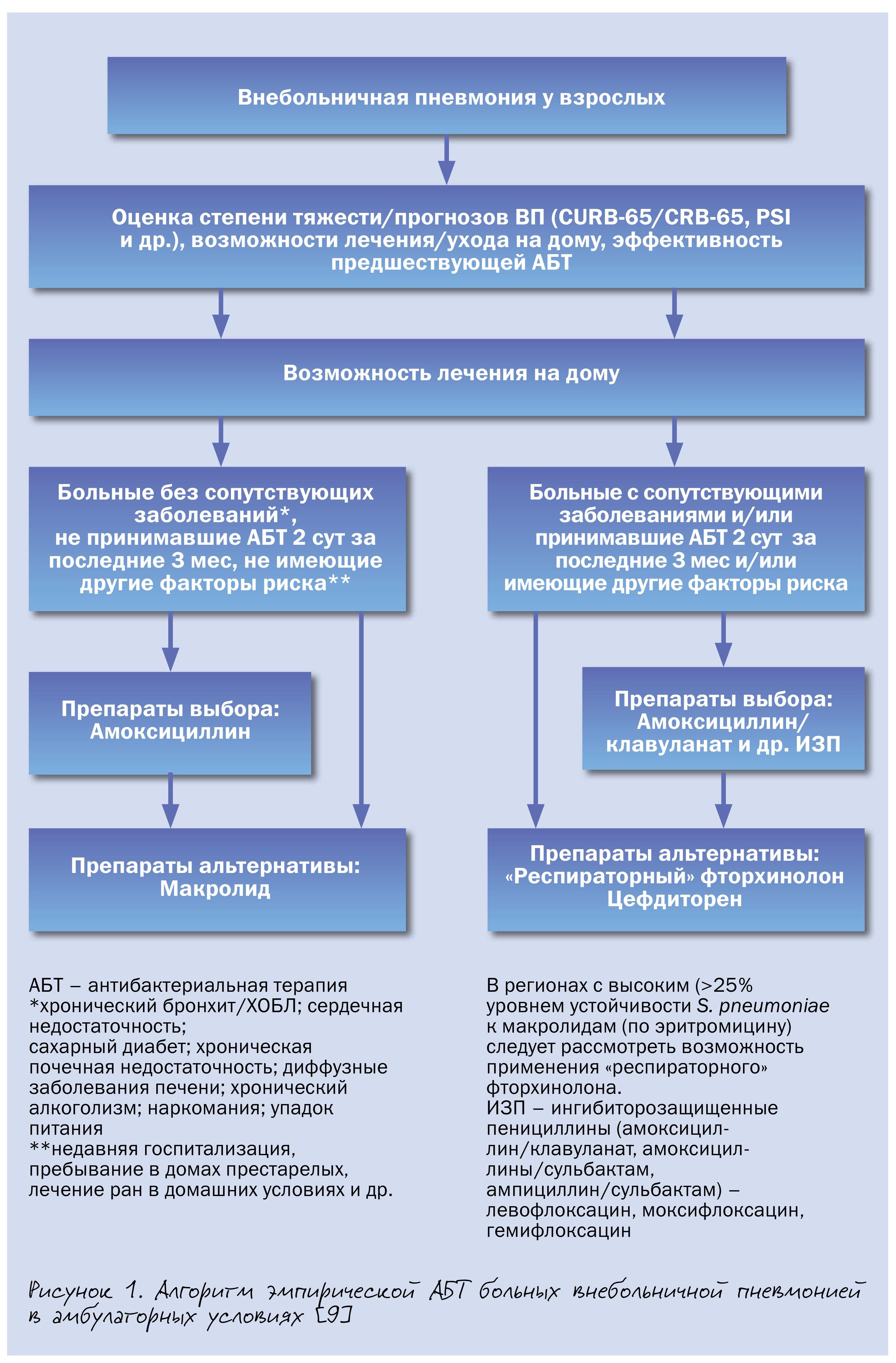
В данной клинической ситуации антибиотиком выбора является амоксициллин, альтернативы – макролиды. Последнее объясняется быстрым и существенным ростом устойчивости S. pneumoniae к макролидам в РФ и, как следствие этого, риском клинических неудач. Макролиды применяют, когда невозможно назначить амоксициллин (индивидуальная непереносимость, анамнестические указания на аллергические реакции немедленного типа на прием β-лактамов), а также при ВП микоплазменной или хламидийной этиологии.
Во вторую группу включены больные внебольничной пневмонией с сопутствующими заболеваниями (ХОБЛ, сахарный диабет, хроническая сердечная недостаточность, хроническая болезнь почек со снижением скорости клубочковой фильтрации, цирроз печени, алкоголизм, наркомания, истощение) и/или принимавшими за последние 3 мес. антибиотики в течение ≥2 последовательных дней и/или имеющими иные факторы риска инфицирования редкими и/или полирезистентными возбудителями. Поскольку вероятность этиологической роли грамотрицательных бактерий (в т. ч. обладающих некоторыми механизмами вторичной лекарственной устойчивости) у этих больных возрастает, то в качестве антибиотиков выбора рекомендуются ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.), а альтернативы – «респираторные» фторхинолоны и цефдиторен.
Подобный подход, предполагающий применение фторхинолонов в качестве альтернативной терапии, является общепринятым и обусловлен необходимостью уменьшить селекцию лекарственноустойчивых штаммов пневмотропных возбудителей и возможность их использования при неэффективности АБТ первого ряда. Несмотря на определенную роль «атипичных» возбудителей в этиологии внебольничной пенвмонии у пациентов данной группы, рутинное назначение комбинации β-лактамного антибиотика и макролида не рекомендуется, так как на сегодняшний день не доказано, что такая стратегия улучшает исходы лечения при возможном увеличении риска нежелательных лекарственных реакций и селекции антибиотикорезистентности.
При госпитализации пациента с внебольничной пневмонией прежде всего необходимо решить вопрос о месте лечения – отделение общего профиля или ОИТ. Крайне важно быстро выявить признаки тяжелой внебольничной пневмонии (табл. 2), так как данные пациенты требуют неотложной помощи в условиях ОИТ.
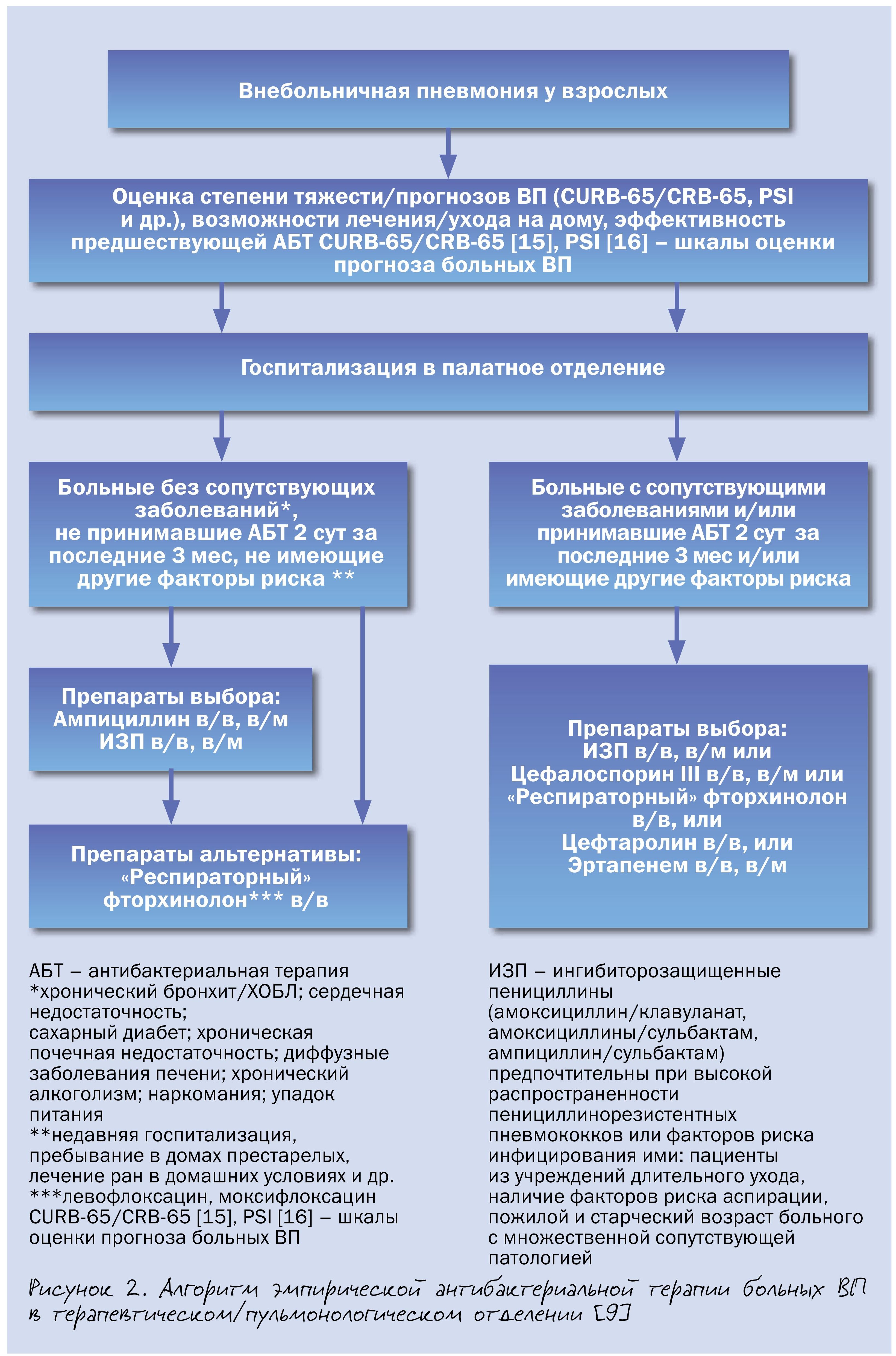
У госпитализированных пациентов возможно применение широкого круга АБТ – ампициллина, ингибиторозащищенных пенициллинов (амоксициллин/клавуланат и др.), цефалоспоринов с высокой антипневмококковой активностью (цефотаксим, цефтриаксон, цефтаролин), эртапенема, «респираторных» фторхинолонов, демонстрирующих в целом сопоставимую эффективность. Стратификация больных аналогична таковой для амбулаторных пациентов.Антибиотиками выбора у госпитализированных больных с нетяжелой ВП без сопутствующих заболеваний и других факторов риска инфицирования редкими и/или полирезистентными возбудителями является ампициллин, альтернативными – ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.) и «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин).
Антибиотиками выбора у госпитализированных больных с нетяжелой ВП при сопутствующих заболеваниях и других факторов риска инфицирования редкими и/или полирезистентными возбудителями будут ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.), цефалоспорины III поколения (цефотаксим, цефтриаксон), «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин), а у отдельных категорий пациентов – цефтаролин и эртапенем. Несмотря на различия в спектре активности in vitro эффективность указанных режимов АБТ у данной категории пациентов сопоставима.
В регионах с высокой распространенностью пенициллинорезистентных пневмококков (ПРП), при наличии индивидуальных факторов риска инфицирования ПРП определенные преимущества может иметь цефтаролин. У пожилых пациентов с множественной сопутствующей патологией и высоким риском неблагоприятного прогноза, наличии факторов риска аспирации, обитателей домов престарелых более эффективно назначение эртапенема.
Имеющиеся доказательства превосходства комбинации «β-лактам + макролид» над монотерпией β-лактамами у госпитализированных больных ВП, полученные преимущественно в рамках обсервационных исследований, касаются, главным образом, тяжелого течения заболевания. Поэтому рутинное назначение комбинированной АБТ при нетяжелой ВП у госпитализированных пациентов нецелесообразно в связи с риском селекции антибиотикорезистентности (рис. 2).

Алгоритм эмпирической антибиотикотерапии больных с тяжелым течением внебольничной пневмонией представлен на рис. 3, однако детальное обсуждение вопросов ведения данной категории пациентов не входило в задачи настоящей статьи.
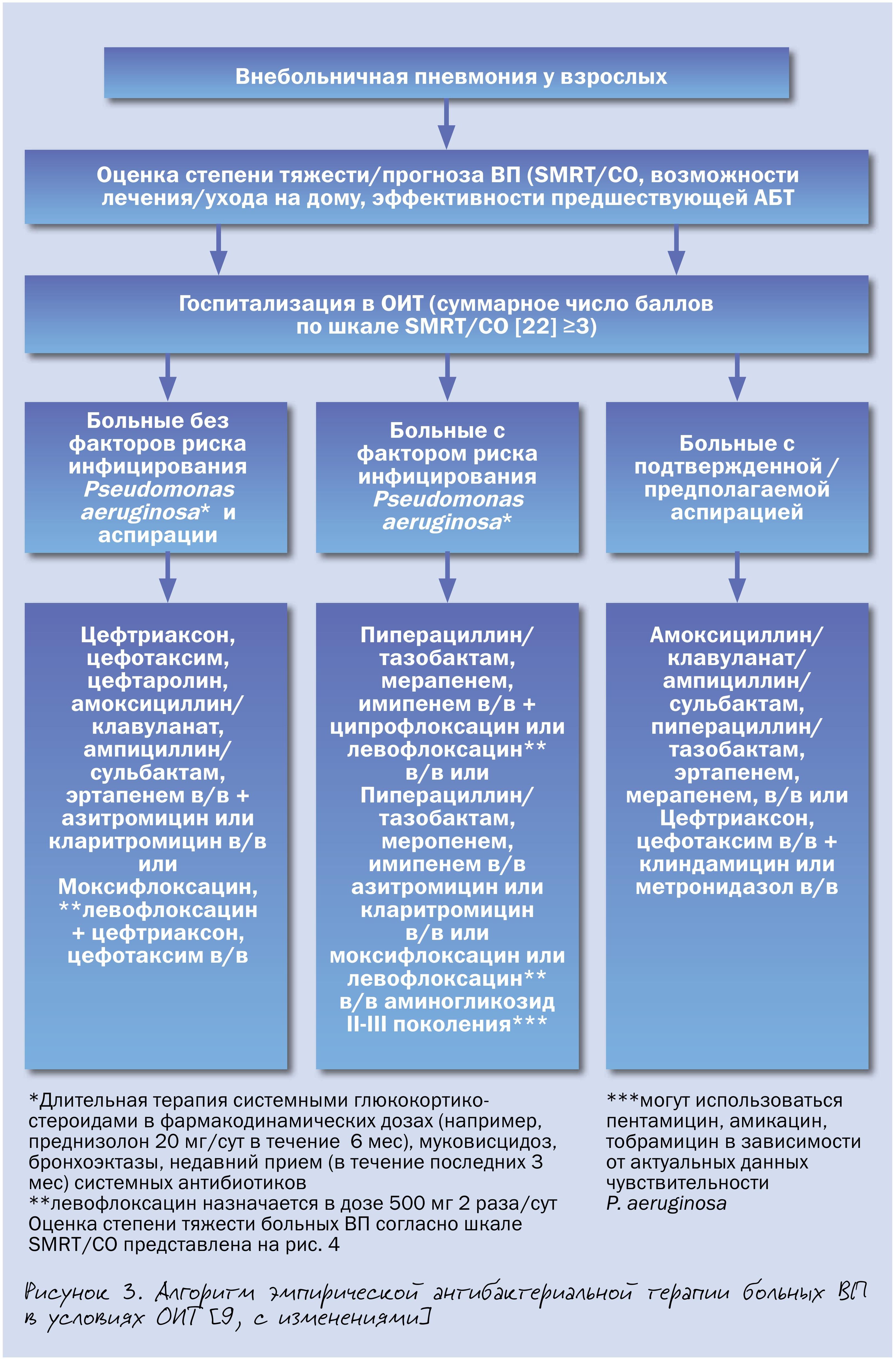
Алгоритмизация как определенная последовательность врачебных действий, представляющихся оптимальными, может оказаться весьма полезной, особенно на начальном этапе ведения больного ВП, когда врач испытывает известный информационный дефицит (этиология заболевания? чувствительность возбудителя ВП к антибиотикам? возможные осложнения ВП? «ответ» пациента на введение первых доз антибиотика? и др.).

Доказательством этому являются, в частности, многочисленные свидетельства того, что следование клиническим рекомендациям, приближающим нас к диагностическому и лечебному универсализму, минимизирует стоимость лечения, сокращает сроки госпитализации и сопровождается снижением летальности. Вместе с тем доступность диагностических и терапевтических алгоритмов не освобождает нас от «индивидуального прочтения» актуальной клинической ситуации в отдельно взятой стране или регионе с учетом локальной антибиотикорезистентности, географической вариабельности этиологии внебольничной пневмонии, сложившихся лечебных традиций (но не укоренившихся заблуждений), и особенностей организации медицинской помощи на амбулаторном и госпитальном этапах. Иными словами, широкая популяризация клинических рекомендаций или их отдельных элементов (включая диагностические и лечебные алгоритмы) вовсе не означает утраты врачом разумной автономии.Источники:
Книги:
Нозокомиальная пневмония у взрослых. 2-е издание
Презентация:
Внебольничная пневмония
Внебольничная пневмония
Внебольничная пневмония
Пневмонии
14.01.2020 | 21:11:58
Источник

Внебольничная пневмония — это заболевание инфекционного происхождения, нижних отделов дыхательных путей (ещё её принято называть внебольничная нижнедолевая пневмония), которое диагностируют и у взрослых, и у детей. При неправильном или несвоевременном лечении может наступить смерть. Это тип пневмонии, не связан с пребыванием больного в лечебном учреждении.
Диагностический минимум обследования больного при внебольничной пневмонии
Помимо сбора жалоб, анамнеза и физикального обследования, диагностический минимум при подозрении на пневмонию должен включать исследования, позволяющие установить точный диагноз и решить вопрос о тяжести течения и месте лечения пациента (терапевтическое отделение или реанимация). К ним относятся:
- рентгенография органов грудной клетки в двух проекциях (передней и боковой);
- общий анализ крови (ОАК);
- биохимический анализ крови — мочевина, креатинин, ионный состав (K, Na), печеночные показатели (АСТ, АЛТ, билирубин);
- микробиологическая диагностика мокроты:
— микроскопия мокроты окрашенного по Граму препарата;
— бактериологический посев мокроты для выделения возбудителя и оценки его чувствительности к антибиотикам (антибиотикограмма);
— исследование гемокультуры (оптимально проводить забор двух проб венозной крови из разных вен с интервалом 30-60 минут.
При тяжелой пневмонии целесообразно исследовать газы артериальной крови (PO2, pCO2) для уточнения потребности в проведении ИВЛ, исключения метаболического, респираторного ацидоза/алкалоза. При наличии плеврального выпота следует произвести плевральную пункцию (плевроцентез, торакоцентез) и исследовать плевральную жидкость (цитологическое, биохимическое и микробиологическое исследование). Наличие 100 мл выпота в плевральной полости не является показанием для пункции.
Критерии тяжелого течения пневмонии и необходимость проведения интенсивной терапии в условиях реанимации/реанимационного отделения
При поступлении больного с внебольничной пневмонией в стационар необходимо прежде всего оценить тяжесть состояния пациента и решить вопрос о госпитализации в профильное отделение терапевтическое или реанимационное.
К тяжелой внебольничной пневмонии обычно относят случаи заболевания, требующие лечения в отделениях реанимации и интенсивной терапии (ОРИТ). Данное определение не совсем точно характеризует данное состояние, так как в разных странах обычно имеются различия в критериях госпитализации больных с бронхо-легочной патологией в ОРИТ. Более точным будет следующее определение тяжелой внебольничной пневмонии:
Тяжелая внебольничная пневмония — это особая форма заболевания различной этиологии, проявляющаяся выраженной дыхательной недостаточностью и/или признаками тяжелого сепсиса или септического шока, характеризующаяся плохим прогнозом и требующая проведение интенсивной терапии.
Выделение больных с тяжелой внебольничной пневмонией в отдельную группу представляется крайне важно, учитывая высокий уровень летальности, наличие, как правило, у пациентов тяжелой фоновой патологии, особенности этиологии заболевания и особые требования к антибактериальной терапии. При внебольничной пневмонии крайне важным является проведение быстрой оценки тяжести состояния больных с целью выделения пациентов, требующих проведения неотложной интенсивной терапии.
Критерии тяжелого течения пневмонии — для оценки пневмонии как тяжелой необходимо наличие хотя бы одного критерия из таблицы:
| Клинические критерии тяжелой пневмонии | Лабораторные критерии тяжелой пневмонии |
|---|---|
|
|
При наличии клинических или лабораторных признаков тяжелой пневмонии или симптомов тяжелого сепсиса целесообразно проводить лечения пациента в отделении реанимации.
Выбор стартовой антибактериальной терапии при пневмонии
Бактериальный или вирусный рост в дистальных отделах дыхательных путей и связанный с ним воспалительный ответ приводят к повреждению клеток, что ухудшает газообмен, изменяет кровообращение в легких и препятствует нормальной механике дыхания.
В случае бактериальной пневмонии первичное повреждение клеток происходит из-за прямого воздействия токсинов, секретируемых бактериями, и токсинов, находящихся на поверхности бактерии. Иногда пневмония с поздним началом, вызванная вирусной инфекцией, не отличима от бактериального заболевания. Для специфического вирусного тестирования существует несколько высокочувствительных, высокоспецифичных анализов на основе полимеразной цепной реакции и иммуноферментного анализа, и во многих клиниках теперь проводится комплексное экспресс-тестирование одного образца аспирированной мокроты, полученной из глотки.
Независимо от возраста начала заболевания при подозрении на бактериальную пневмонию лечение необходимо начинать немедленно с эмпирического антибактериального режима, при этом антибиотик должен иметь достаточно широкий спектр действия, чтобы воздействовать на наиболее вероятные этиологические микроорганизмы, в том числе те, которые могут быть резистентными к лекарственным средствам.
То есть при бактериальной пневмонии выбор антибиотика проводят эмпирически, а замену на альтернативный препарат проводят по результатам бактериологического исследования или эмпирически при первых признаках неэффективности — в течение 24-36 ч.
У госпитализированных больных подразумевается более тяжелое течение пневмонии, поэтому целесообразно начинать терапию с парентеральных антибиотиков. Через 3-4 дня лечения при достижении клинического эффекта (нормализация температуры, уменьшение выраженности интоксикации и других симптомов заболевания), возможен переход с парентерального на пероральный способ применения антибиотика до завершения полного курса антибактериальной терапии. При легком течении пневмонии у госпитализированных больных допускается сразу назначение антибиотиков внутрь.
Рекомендации по эмпирической терапии пневмонии у госпитализированных больных представлены в таблице ниже. Режим дозирования антибактериальных препаратов необходимо подбирать индивидуально в соответствии с рекомендованной дозой, указанной в инструкции к препарату от производителя.
Антибактериальная терапия пневмоний у госпитализированных больных
| Особенности нозологической формы | Наиболее актуальные возбудители | Рекомендованные режимы терапии | Комментарии |
|---|---|---|---|
| Пневмония не тяжелого течения | Streptococcus pneumoniae Haemophilus influenzae Chlamydia pneumonia Staphylococcus aureus Enterobacteriaceae | Ампициллин в/в Амоксициллин/клавуланат в/в Цефуроксим в/в Цефотаксим в/в Цефтриаксон в/в | Возможна ступенчатая терапия. При стабильном состоянии пациента допускается сразу назначение препаратов внутрь в таблетированной форме или суспензии. |
| Пневмония тяжелого течения | Streptococcus pneumoniae Legionella spp. Staphylococcus aureus Enterobacteriaceae | Препараты выбора: Амоксициллин/клавуланатв/в+макролид в/в Цефотаксим+макролидв/в Цефтриаксон+макролид в/в Альтернативные средства: Ранние фторхинолоны (ципрофлоксацин, офлоксацин) + цефалоспорины III поколения Новые фторхинолоны (левофлоксацин, моксифлоксацин) |
У госпитализированных больных с не тяжелой внебольничной пневмонией рекомендуется применение парентеральных аминопенициллинов или защищенных аминопенициллинов, парентеральных цефалоспоринов II-III поколения. Клинических данных о преимуществе какого-либо из указанных антибактериальных препаратов или о присоединении на первом этапе лечения макролидных антибиотиков нет.
При тяжелой внебольничной пневмонии средствами выбора являются парентерально вводимые защищенные пенициллины или цефалоспорины III поколения в комбинации с макролидами для парентерального введения (эритромицин, кларитромицин, спирамицин). Указанные комбинации перекрывают практически весь спектр потенциальных возбудителей (как типичных, так и атипичных) тяжелой пневмонии.
Имеются данные о высокой клинической эффективности парентеральных фторхинолонов (ципрофлоксацин, офлоксацин) при тяжелых внебольничных пневмониях. Однако эти препараты характеризуются слабой антипневмококковой активностью по сравнению с бета-лактамами, описаны случаи неуспеха терапии ранними фторхинолонами пневмококковой пневмонии. Вопрос о месте ранних фторхинолонов в лечении тяжелой внебольничной пневмонии окончательно не решен, более надежной является их комбинация с бета-лактамами. Потенциально перспективными являются новые фторхинолоны (левофлоксацин, моксифлоксацин) для парентерального применения, обладающие повышенной антипневмококковой активностью и перекрывающие практически весь спектр возможных возбудителей. Имеются данные контролируемых клинических исследований о возможности применения новых фторхинолонов при тяжелой внебольничной пневмонии в режиме монотерапии.
Критерии эффективности антибактериальной терапии внебольничной пневмонии
Первоначальная оценка эффективности антибактериальной терапии должна проводится через 48-72 часа после начала лечения. Основными критериями эффективности в эти сроки являются снижение интоксикации и температуры, отсутствие дыхательной недостаточности. Если у пациента сохраняется высокая лихорадка и интоксикация, или симптоматика прогрессирует, то лечение следует признать неэффективным и произвести замену режима антибактериальной терапии. Рекомендации по смене режима антибактериальной терапии приведены ниже в таблице.
Выбор антибактериального препарата при неэффективности стартового режима терапии у госпитализированных больных
| Препараты на первом этапе лечения | Препараты на втором этапе лечения | Комментарии |
|---|---|---|
| Ампициллин | Заменить на или присоединить макролидный антибиотик При тяжелой пневмонии заменить на цефалоспорин III поколения + макролид | Возможны атипичные микроорганизмы — микоплазма, хламидия, легионелла |
| Амоксициллин/клавуланат Цефуроксим | Присоединить макролидный антибиотик | Возможны атипичные микроорганизмы — микоплазма, хламидия, легионелла |
| Цефалоспорины III поколения | Присоединить макролидный антибиотик | Возможны атипичные микроорганизмы — микоплазма, хламидия, легионелла |
При неэффективности антибактериальной терапии на втором этапе необходимо провести обследование больного для уточнения диагноза или выявления возможных осложнений пневмонии. При тяжелой пневмонии оптимальным будет проведение МСКТ органов грудной клетки с целью исключения хирургической патологии.
В процессе лечения с целью оценки состояния пациента и эффективности терапии целесообразно осуществлять следующие исследования:
- Общий анализ крови — на 2-3-й день и после окончания антибактериальной терапии;
- Биохимический анализ крови — контроль через 1 неделю при наличии изменений в первом исследовании;
- Исследование газов крови (при тяжелом течении) — ежедневно до нормализации показателей;
- Рентгенография грудной клетки — через 2-3 недели после начала лечения (перед выпиской); при ухудшении состояния пациента — в более ранние сроки.
Продолжительность антибактериальной терапии
При нетяжелой внебольничной пневмонии антибактериальная терапия может быть завершена по достижении стойкой нормализации температуры тела (в течение 3-4 дней). При таком подходе длительность лечения обычно составляет 7-10 дней. При этом курс антибиотикотерапии должен быть не менее 7 дней. В эти же сроки обычно наблюдается исчезновение лейкоцитоза по анализу крови. В случае наличия клинических и/или эпидемиологических данных о микоплазменной или хламидийной этиологии пневмонии продолжительность терапии должна составлять 14 дней, хотя имеются клинические данные об эффективности и более коротких курсов антибактериальной терапии при атипичной пневмонии. Более длительные курсы антибактериальной терапии показаны при пневмонии стафилококковой этиологии или вызванной грамотрицательными энтеробактериями — от 14 до 21 дня. При указании на легионеллезную пневмонию длительность антибактериальной терапии составляет 21 день.
Критерии эффективности (достаточности) антибактериальной терапии пневмонии:
- Температура ниже 37,5°С
- Отсутствие интоксикации
- Отсутствие дыхательной недостаточности (частота дыхания менее 20 вдохов в минуту)
- Отсутствие гнойной мокроты
- Количество лейкоцитов в крови меньше 10·109/Л, нейтрофилов меньше 80%, юных форм меньше 6%
- Отсутствие отрицательной динамики на рентгенограмме органов грудной клетки.
Сохранение отдельных клинических, лабораторных или рентгенологических признаков пневмонии не является абсолютным показанием к продолжению антибактериальной терапии или ее модификации. В подавляющем большинстве случаев их разрешение происходит самостоятельно или под влиянием симптоматической терапии. Длительно сохраняющийся субфебрилитет не является признаком бактериальной инфекции, а, скорее всего, является проявлением постинфекционной астении.
Рентгенологическая динамика отмечается медленнее по сравнению с клинической картиной, поэтому контрольная рентгенография грудной клетки не может служить критерием для определения длительности антибактериальной терапии.
Вместе с тем при длительно сохраняющейся клинической, лабораторной и рентгенологической симптоматики пневмонии необходимо провести дифференциальную диагностику с такими заболеваниями, как рак легкого, туберкулез, застойная сердечная недостаточность и др.
Ступенчатая антибактериальная терапия пневмонии
Ступенчатая антибактериальная терапия предполагает двухэтапное применение антибактериальных препаратов: переход с парентерального на пероральный путь введения в возможно более короткие сроки с учетом клинического состояния пациента. Основная идея ступенчатой терапии заключается в уменьшении длительности парентерального введения антибиотика, что обеспечивает значительное уменьшение стоимости лечения и сокращение срока пребывания больного в стационаре при сохранении высокой клинической эффективности терапии.
Оптимальным вариантом ступенчатой терапии является последовательное использование двух лекарственных форм (для парентерального введения и приема внутрь) одного и того же антибактериального препарата, что обеспечивает преемственность лечения. Возможно последовательное применение антибактериальных препаратов, близких по своим антимикробным свойствам и одинаковым уровнем приобретенной устойчивости. Антибиотик для перорального введения должен удовлетворять следующим требованиям: высокая биодоступность при приеме внутрь, отсутствие лекарственных взаимодействий, хорошая переносимость, длительный интервал между приемом, приемлемая стоимость.
Переход с парентерального на пероральный способ применения антибиотика следует осуществлять при стабилизации состояния пациента и улучшении клинической картины пневмонии. При этом целесообразно использовать следующие критерии:
- нормальная температура тела (<37,5°C) при двух последовательных измерениях с интервалом 8ч;
- уменьшение одышки;
- отсутствие нарушения сознания;
- положительная динамика других симптомов заболевания;
- отсутствие нарушений гастроинтестинальной абсорбции;
- согласие (настроенность) пациентов на пероральное лечение.
На практике возможность перехода на пероральный способ введения антибиотика появляется в среднем через 2-3 дня после начала лечения.
Перечень антибиотиков, выпускаемых в лекарственных формах, предназначенных для парентерального и перорального применения и используемых для ступенчатой терапии достаточно широк:
- амоксициллин/клавуланат,
- кларитромицин,
- левофлоксацин,
- моксифлоксацин,
- офлоксацин,
- спирамицин,
- цефуроксим натрия — цефуроксим аксетил,
- ципрофлоксацин,
- эритромицин.
Для некоторых антибиотиков, не имеющих лекарственной формы для перорального применения, возможна замена на близкие по антимикробному спектру препараты с учетом чувствительности выявленного возбудителя пневмонии.
В сложившихся современных условиях особую важность приобретают своевременная микробиологическая верификация заболевания, оценка чувствительности возбудителя к антимикробным препаратам, а также разработка программ профилактики.
ПРОГНОЗ
При несвоевременном и неправильном лечении пневмония может закончиться развитием сегментарного или долевого пневмосклероза и деформаций бронхов в зоне поражения, однако такие исходы в настоящее время сейчас наблюдают крайне редко, обычно у людей с хроническими болезнями лёгких (муковисцидоз, пороки развития и др.). Большинство пневмоний рассасывается бесследно, усиление и деформация лёгочного рисунка, которые могут сохраняться в течение нескольких месяцев, не требует ни уточняющих исследований (например, КТ), ни лечения.
Статистика
- В среднем пациенты госпитализируются в стационар в сроки от трех до десяти дней.
- Обнаружено преимущественно правостороннее поражение легких.
- Чаще внебольничная пневмония имеет cреднюю степень тяжести.
- Пневмония вирусной этиологии имеет тяжелое, осложненное течение и заканчивается летальным исходом.
- В России для лечения внебольничной пневмонии чаще всего применяют комбинацию цефалоспоринов и аминогликозидов и сочетание цефалоспоринов и макролидов.
Данные проверены и актуальны на декабрь 2019 года
Литература:
Таточенко В. К., Самсыгина Г. А., Синопальников А. И., Учайкин В. Ф. Пневмония // ПФ. 2006. №4.
Внебольничная пневмония у взрослых: диагностика, лечение, профилактика. ПРОЕКТ ПРАКТИЧЕСКИХ РЕКОМЕНДАЦИЙ. Москва — 2002.
Фесенко О.В., Швайко С.Н. Пневмонии, вызванные Klebsiella pneumoniae (фридлендеровские пневмонии) // Практическая пульмонология. 2019.
Хувен Т.А., Полин Р.А. Пневмония // Неонатология: Новости. Мнения. Обучение. 2017. №3
Афтаева Лариса Николаевна, Мельников Виктор Львович, Кубрина Ольга Юрьевна, Орешкина Анастасия Александровна Особенности течения внебольничных пневмоний // Вестник ПензГУ. 2019. №1 (25).
Сохранить в соцсетях:
Похожие публикации:
Ваш отзыв:

Карточка данной публикации. Тема: «Внебольничная пневмония: лечение антибиотиками», опубликована в разделе Лекарства — последняя редакция, обновление: 2019-12-11
Копирование информации возможно с обязательной ссылкой на krasgmu.net!
Раздел
: Лекарства |
|
Просмотров
: 837
Нашли ошибку? Есть свои предложения? Сообщите нам
Источник

