Схема антибактериальной терапии внебольничной пневмонии

Американское общество по инфекционным болезням (IDSA) и Американское торакальное общество (ATS) опубликовали основные принципы клинической практики при внебольничной пневмонии (ВП) у взрослых (октябрь 2019 года).
Краткое изложение рекомендаций без анализа и комментариев.
Диагностика
Диагноз внебольничной пневмонии является определенным при наличии у больного рентгенологически подтвержденной очаговой инфильтрации легочной ткани и, по крайней мере, двух клинических признаков из числа следующих: а) остролихорадочное начало заболевания (Т > 38, 0°С) ; б) кашель с мокротой; в) физические признаки (фокус крепитации и/или мелкопузырчатых хрипов, жесткого/бронхиального дыхания, укорочения перкуторного звука) ; г) лейкоцитоз (>10·109/л) и/или палочкоядерный сдвиг (>10%). При этом необходимо учитывать и возможность известных синдромосходных заболеваний/патологических состояний.
Окраска по Граму и посев мокроты
Рутинный посев мокроты и окраска по Граму не рекомендованы для взрослых амбулаторных больных с внебольничной пневмонией.
У госпитализированных пациентов предварительная окраска по Граму и посев секрета дыхательных путей рекомендуются для взрослых с ВП, которая считается тяжелой (особенно у интубированных пациентов) или если ВП удовлетворяет одному из следующих условий:
- в настоящее время пациент проходит эмпирическое лечение метициллин-резистентного золотистого стафилококка (MRSA) или Pseudomonas aeruginosa.
- ранее имела место инфекция MRSA или P. aeruginosa , особенно инфекция дыхательных путей.
- пациент был госпитализирован в течение предшествующих 90 дней и по любой причине получал парентеральные антибиотики.
Культура крови
Посев крови не рекомендуется проводить у взрослых амбулаторных больных с ВП.
Рутинные посевы крови не рекомендуются для госпитализированных взрослых пациентов с ВП.
Посевы крови перед лечением рекомендуются проводить для госпитализированных взрослых пациентов с ВП, которая классифицируется как тяжелая, или которая отвечают одному из следующих условий:
- В настоящее время проходит эмпирическое лечение MRSA или P aeruginosa
- Ранее была инфекция MRSA или P aeruginosa , особенно дыхательных путей
- Был госпитализирован в течение предшествующих 90 дней и по любой причине получал парентеральные антибиотики.
Анализ на антиген Legionellа и пневмококкового антигена в моче
Рутинное исследование мочи на наличие пневмококкового антигена не рекомендуется у взрослых с ВП, кроме случаев, когда ВП является тяжелой.
Рутинное тестирование мочи на наличие антигена Legionella не рекомендуется у взрослых с ВП, за исключением случаев, когда ВП является тяжелой или есть указание на предрасполагающие эпидемиологические факторы (например, вспышка Legionella или недавние путешествия).
Тестирование на Legionella должно состоять из оценки мочевого антигена и сбора секреции нижних дыхательных путей для культивирования на селективных средах или амплификации нуклеиновых кислот (ПЦР-диагностика).
Тестирование на грипп
Если в обществе циркулирует вирус гриппа, рекомендуется проводить тестирование на грипп у взрослых пациентов с ВП.
Определение прокальцитонина
Эмпирическая антибиотикотерапия рекомендуется взрослым пациентам с клинической картиной ВП и рентгенологически подтвержденным диагнозом ВП независимо от исходного уровня прокальцитонина в сыворотке крови пациента.
Лечение
Решение о госпитализации
Решение о госпитализации у взрослых с ВП должно базироваться прежде всего на оценке степени тяжести заболевания (предпочтительно использовать шкалу PSI (Community-Acquired Pneumonia Severity Index (PSI) for Adults).
Прямое поступление в отделение реанимации рекомендуется для пациентов с ВП, у которых есть гипотония, требующая вазопрессорной поддержки или дыхательная недостаточность, требующая искусственной вентиляции легких.
Амбулаторные схемы лечения антибиотиками
Антибиотики, рекомендованные для взрослых пациентов с ВП, которые в остальном здоровы:
- Амоксициллин 1 г три раза в день ИЛИ
- Доксициклин 100 мг два раза в день ИЛИ
- В областях с пневмококковой устойчивостью к макролидам <25%: макролид (азитромицин 500 мг в первый день и затем 250 мг в день или кларитромицин 500 мг два раза в день или кларитромицин пролонгированого высвобождения 1000 мг в день)
Для амбулаторных взрослых с ВП, у которых есть сопутствующие заболевания, рекомендуются следующие схемы приема антибиотиков:
- Комбинированная терапия:
- Амоксициллин / клавуланат 500 мг / 125 мг 3 раза в день ИЛИ амоксициллин / клавуланат 875 мг / 125 мг два раза в день ИЛИ 2000 мг / 125 мг два раза в день ИЛИ цефалоспорин (цефподоксим 200 мг два раза в день или цефуроксим 500 мг два раза в день) ПЛЮС
- Макролид (азитромицин 500 мг в первый день, затем 250 мг в день, кларитромицин [500 мг два раза в день или пролонгированного высвобождения 1000 мг один раз в день] ) или доксициклин 100 мг два раза в день ИЛИ
- Монотерапия: респираторный фторхинолон (левофлоксацин 750 мг в день, моксифлоксацин 400 мг в день или гемифлоксацин 320 мг в день)
Стационарные схемы лечения антибиотиками
Следующие эмпирические схемы лечения рекомендуются взрослым пациентам с нетяжелой формой ВП, у которых нет факторов риска MRSA или P. aeruginosa :
- Комбинированная терапия бета-лактамом (ампициллин плюс сульбактам 1, 5–3 г каждые 6 часов, цефотаксим 1-2 г каждые 8 часов, цефтриаксон 1-2 г ежедневно или цефтаролин 600 мг каждые 12 часов) и макролидом (азитромицин 500 мг ежедневно или кларитромицин 500 мг два раза в день) ИЛИ
- Монотерапия дыхательным фторхинолоном (левофлоксацин 750 мг в день, моксифлоксацин 400 мг в день)
Следующие схемы рекомендуется для взрослых пациентов с тяжелой ВП без факторов риска MRSA или P. aeruginosa :
- Бета-лактам плюс макролид ИЛИ
- Бета-лактам плюс респираторный фторхинолон
Использование антибактериальных препаратов, активных в отношении анаэробных микроорганизмов при подозрении на аспирационную пневмонию не рекомендуется, за исключением случаев, когда подозревается абсцесс легкого или эмпиема.
Антибактериальная терапия препаратами расширенного спектра в отношении MRSA или P. aeruginosa
Эмпирическое назначение антибиотиков, активных в отношении MRSA или P. aeruginosa рекомендуется для взрослых пациентов с ВП только при наличии локально подтвержденных факторов риска.
Эмпирические варианты лечения MRSA включают ванкомицин (15 мг/кг каждые 12 часов) или линезолид (600 мг каждые 12 часов).
Эмпирические варианты лечения P. aeruginosa включают пиперациллин-тазобактам (4, 5 г каждые 6 часов), цефепим (2 г каждые 8 часов), цефтазидим (2 г каждые 8 часов), азтреонам (2 г каждые 8 часов), меропенем (1 г каждый) 8 часов) или имипенем (500 мг каждые 6 часов).
Эмпирическая терапия с учетов возможности наличия MRSA или P. aeruginosa продолжается до получения лабораторных культуральных данных.
Кортикостероидная терапия
Рутинное назначение кортикостероидов не рекомендуется у взрослых пациентов с ВП или при тяжелой пневмонией на фоне гриппа. Одобрено их применение у пациентов с рефрактерным септическим шоком.
Противогриппозная терапия
Противогриппозное лечение (например, осельтамивир) следует назначать всем взрослым с ВП, у которых тест на грипп положительный.
Антибактериальная терапия у больных гриппом
Стандартное антибактериальное лечение следует изначально назначать взрослым с клиническими и рентгенологическими признаками ВП, у которых тест на грипп положительный.
Продолжительность лечения
Продолжительность антибиотикотерапии должна основываться на клинических данных в виде стабилизации состояния пациента и продолжаться не менее 5 дней после достижения клинического улучшения.
Критерии достаточности антибактериальной терапии пневмонии:
- Температура < 37, 5°С
- Отсутствие интоксикации
- Отсутствие дыхательной недостаточности (частота дыхания менее 20 в минуту)
- Отсутствие гнойной мокроты
- Количество лейкоцитов в крови < 10 х 109/Л, нейтрофилов < 80%, юных форм < 6%
- Отсутствие отрицательной динамики на рентгенограмме.
Рентгенологическая динамика отмечается медленнее по сравнению с клинической картиной, поэтому контрольная рентгенография грудной клетки не может служить критерием для определения длительности антибактериальной терапии.
Последующая визуализация грудной клетки
Рутинное последующее обследование не рекомендовано для взрослых пациентов с ВП, у которых симптомы купировались в течение 5-7 дней.
Показания для госпитализации
В соответствии с современными подходами к ведению взрослых больных внебольничной пневмонией значительное их число может с успехом лечится на дому. В этой связи особое значение приобретают показания для госпитализации:
- Возраст старше 60-65 лет.
- Наличие сопутствующих заболеваний (хронический бронхит/хроническая обструктивная болезнь легких, бронхоэктазия, злокачественные новообразования, сахарный диабет, хроническая почечная недостаточность, застойная сердечная недостаточность, хронический алкоголизм, наркомания, упадок питания, цереброваскулярные заболевания).
- Госпитализации (по любому поводу), имевшие место в течение последних 12 месяцев.
- Данные физического обследования: частота дыхания ≥ 30/мин; диастолическое артериальное давление ≤ 60 мм рт. ст. ; систолическое артериальное давление < 90 мм рт. ст. ; частота сердечных сокращений ≥ 125/мин; температуры тела < 35, 0°С или ≥ 40, 0°С; нарушения сознания.
- Лабораторные и рентгенологические данные: количество лейкоцитов периферической крови < 4, 0·109/л или > 30, 0·109/л; SaO2 < 92% (по данным пульсоксиметрии), РаО2 < 60 мм рт. ст. и/или РаСО2 > 50 мм рт. ст. при дыхании комнатным воздухом; креатинин сыворотки крови > 176, 7 мкмоль/л или азот мочевины > 7, 0 ммоль/л (азот мочевины = мочевина, ммоль/л / 2, 14) ; пневмоническая инфильтрация, локализующаяся более чем в одной доле; наличие полости (полостей) распада; плевральный выпот; быстрое прогрессирование очагово-инфильтративных изменений в легких (увеличение размеров инфильтрации > 50% в течение ближайших 2-х суток) ; гематокрит < 30% или гемоглобин < 90 г/л; внелегочные очаги инфекции (менингит, септический артрит и др. ) ; сепсис или полиорганная недостаточность, проявляющаяся метаболическим ацидозом (рН < 7, 35), коагулопатией.
- Невозможность адекватного ухода и выполнения всех врачебных предписаний в домашних условиях.
- Предпочтения пациента и/или членов его семьи.
Источник:
Metlay JP, Waterer GW, Long AC, Anzueto A, Brozek J, Crothers K, et al. Diagnosis and Treatment of Adults with Community-acquired Pneumonia. An Official Clinical Practice Guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med. 2019 Oct 1. 200 (7):e45-e67.
https://www.iacmac.ru/rus/all/metod/pneumonia/08.shtml
https://www.iacmac.ru/rus/all/metod/pneumonia/09.shtml
Статья добавлена 21 января 2020 г.
Источник
СОДЕРЖАНИЕ
ОБЩИЕ СВЕДЕНИЯ
ВАЖНО ЗНАТЬ
ТАКТИКА И СТРАТЕГИЯ ЛЕЧЕНИЯ ПНЕВМОНИИ У ВЗРОСЛЫХ
ЛЕЧЕНИЕ ПНЕВМОНИИ В СТАЦИОНАРЕ
ЗАКЛЮЧЕНИЕ
Внебольничная пневмония (синонимы: домашняя пневмония, амбулаторная, воспаление легких) — это острое инфекционное заболевание легких, возникшее во внебольничных условиях или в первые 48 часов госпитализации, сопровождающееся симптомами инфекции нижних дыхательных путей (температура, кашель, боли в груди, одышка) и «свежими» очагово-инфильтративными изменениями в легких при отсутствии очевидной диагностической альтернативы. Внебольничная пневмония у взрослых (воспаление легких у взрослых) довольно распространена. По результатам современных эпидемиологических исследований, заболеваемость внебольничной пневмонией у взрослых составляет 3-40%, около 50% из них госпитализируются. При этом каждый 10-й пациент с внебольничной пневмонией в силу тяжелого или осложненного течения заболевания помещается в отделение интенсивной терапии (ОИТ). И если летальность среди амбулаторных больных, как правило, не превышает 0,5 %, то госпитальная летальность достигает 14 % и более.
Согласно данным официальной статистики, заболеваемость пневмонией в РФ в 2018 г. составила 490,6 на 100 тыс., что на 19 % превысило аналогичный показатель, зарегистрированный в 2017 г. (412,3/100 000); отмечен также и рост летальности (на 2,2 %) больных внебольничной пневмонией – с 19,11/100 000 в 2017 г. до 19,8/100 000 в 2018 г.
При этом ведущее место в достижении оптимального исхода у данной категории пациентов занимает своевременно начатая рациональная антибактериальная терапия (АБТ).
Основные вопросы, связанные с антибактериальной терапией (антибиотики при пневмонии):
I. Стратификация пациентов. При выборе антибиотика нужно учитывать факторы риска неблагоприятного исхода и степень тяжести заболевания. Также следует принять во внимание наличие известных факторов риска появления отдельных возбудителей внебольничной пневмонии у взрослых – лекарственноустойчивых Streptococcus pneumoniae 1*, грамотрицательных энтеробактерий *2, Pseudomonas aeruginosa *3.
1*Возраст > 65 лет, терапия β-лактамами в течение последних 3 мес, множественные сопутствующие заболевания внутренних органов (сахарный диабет, сердечная недостаточность, ХОБЛ и др.) и др.
2*Обитатели домов престарелых, проводимая антибактериальная терапия, множественные сопутствующие заболевания и др.
3*«Структурные» заболевания легких (например, бронхоэктазия), системная терапия глюкокортикоидами, упадок питания, терапия антибиотиками широкого спектра действия более 7 дней в течение последнего месяца.
II. Соотношение «цена/эффективность». Идеальный антибиотик – это не самый дешевый препарат. Оценивая прямые затраты на лечение (прежде всего, в амбулаторных условиях), со стоимостью лекарственного средства нужно соотнести длительность нетрудоспособности пациента и частоту терапевтических неудач, в том числе повлекших за собой госпитализацию. Разумеется, что стоимость антибактериальной терапии зачастую несопоставима с последствиями терапевтической неудачи.
III. Приверженность пациента лечебным рекомендациям. Серьезными препятствиями к выполнению пациентом назначений являются: обилие и частота приема лекарственных препаратов, влияние лечения на сложившийся жизненный стереотип и минимальные последствия несоблюдения врачебных рекомендаций в представлении больного.
При решении этих и других вопросов, связанных с антибактериальной терапией, нужно учитывать следующее:
а) традиционные диагностические тесты, направленные на этиологическую верификацию ВП, характеризуются ограниченной ценностью (их результативность не превышает 50 %);
б) антибактериальная терапия пневмонии, по крайней мере в дебюте заболевания, носит эмпирический характер;
в) выбор и время начала АБТ имеют определяющее прогностическое значение;
г) ключевыми возбудителями большинства случаев внебольничной пневмонии являются Streptococcus pneumoniae (пневмококк), Haemophilus influenzae, «атипичные» микроорганизмы (Chlamydophila pneumoniae, Mycoplasma pneumoniae);
д) доказан реальный вклад коинфекции (например, сочетании пневмококка и «атипичных» возбудителей) в развитие внебольничной пневмонии;
е) все более актуальной становится проблема распространения лекарственноустойчивых штаммов основных возбудителей внебольничной пневмонии.
В целом же выбор обоснованной эмпирической антибактериальной терапии внебольничной пневмонии строится на знании ограниченного перечня возбудителей заболевания и предсказуемых уровней резистентности в пределах обширных географических регионов. Так, к числу основных возбудителей внебольничной пневмонией нетяжелого течения, т. е. не требующей госпитализации, относятся S. pneumoniae, M. pneumoniae, C. pneumoniae, тогда как среди микробиологических «находок» у больных с более тяжелым течением заболевания, нуждающихся в госпитализации (в т. ч. в ОИТ), наряду с пневмококком, H. influenzae фигурируют Legionella pneumophila, представители семейства Enterobacteriaceae (прежде всего, Klebsiella pneumoniae, Escherichia coli), Staphylococcus aureus.
В выборе рациональной антибактериальной терапии, помимо ориентированности в этиологии ВП, не менее важно знать структуру лекарственной устойчивости ключевых возбудителей заболевания, и, прежде всего, пневмококка. В некоторых странах устойчивость пневмококков к пенициллину достигает 60 %, причем многие из них обладают резистентностью к трем и более классам антибиотиков. Резистентность S. pneumoniae к пенициллину обычно сочетается с устойчивостью к цефалоспоринам I–II поколений, тетрациклинам, ко-тримоксазолу.
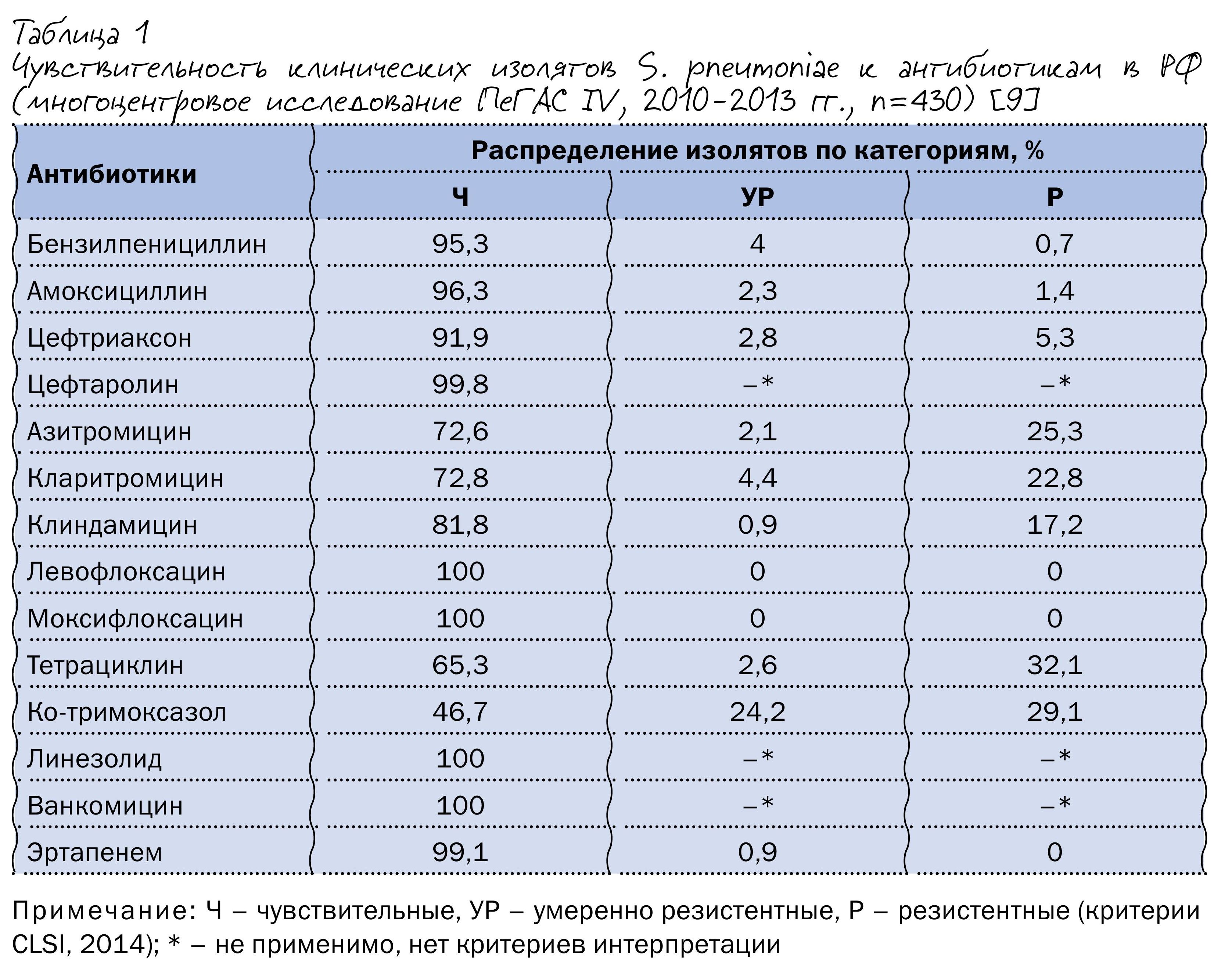
Данные мониторинга чувствительности клинических штаммов S. pneumoniae в РФ, выделенных у пациентов с внебольничными инфекциями нижних дыхательных путей в 2010–2013 гг., представлены в таблице 1. Отличительная черта нашей страны – высокий уровень резистентности пневмококка к тетрациклинам и ко-тримоксазолу, что может быть связано с неоправданно высокой частотой их применения в XX – начале XXI вв. Уровень же устойчивости S. pneumoniae к пенициллину и аминопенициллинам остается относительно невысоким – 4,7 и 1,4 % изолятов соответственно.
Резистентность пневмококка к различным макролидам и линкозамидам варьирует в пределах 18–27,4 %; большинство макролидорезистентных пневмококков демонстрируют устойчивость к клиндамицину, что может свидетельствовать о преобладании в РФ MLSB-фенотипа резистентности, обусловленного модификацией мишени и определяющего устойчивость S. pneumoniae ко всем макролидам, включая 16-членные.
В настоящее время появились доказательства превосходства некоторых подходов к лечению взрослых больных ВП. Так, целесообразность раннего назначения антибиотиков (в первые 4–8 ч от момента госпитализации) подтверждаются результатами обсервационных исследований и согласуется с мнением экспертов.
Для снижения затрат можно использовать современные рекомендации, облегчающие выбор пациентов ВП, которые могли бы безопасно и эффективно лечиться в амбулаторных условиях.
По возможности ранний переход с парентерального введения антибиотика на его прием внутрь и следующая за этим выписка из стационара (когда пациент становится клинически стабильным) также снижает стоимости лечения.
Выбор препаратов для стартовой антибактериальной терапии больных внебольничной пневмонией определяет спектр потенциальных возбудителей заболевания и профиль антибиотикорезистентности. При этом важно иметь в виду, что «…данные, полученные из существующих рандомизированных клинических исследований, не позволяют создать доказательные рекомендации по выбору антибиотика для терапии внебольничной пневмонии». Поэтому стратификация больных и рекомендации по выбору антибактериальной пневмонии в большей степени отражают национальные эпидемиологические данные антибиотикорезистентности ключевых возбудителей внебольничной пневмонии, их потенциальное экологическое влияние, а также учитывают затратную эффективность лекарственной терапии.
Согласно положениям проекта национальных рекомендаций, подготовленных экспертами Российского респираторного общества (РРО) и Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии (МАКМАХ), среди больных пневмонией, которые могут получать лечение в амбулаторных условиях, целесообразно выделять 2 группы. В первую из них включены пациенты без серьезных хронических заболеваний внутренних органов, не принимавшие за последние 3 мес системные антибиотики и не имеющие другие факторы риска инфицирования редкими и/или полирезистентными возбудителями (пребывание в доме престарелых или других учреждениях длительного ухода, наличие госпитализаций по любому поводу в течение ≥2 суток в предшествующие 90 дней, в/в инфузионная терапия, лечение ран в домашних условиях в предшествующие 30 дней и др.) (рис. 1).
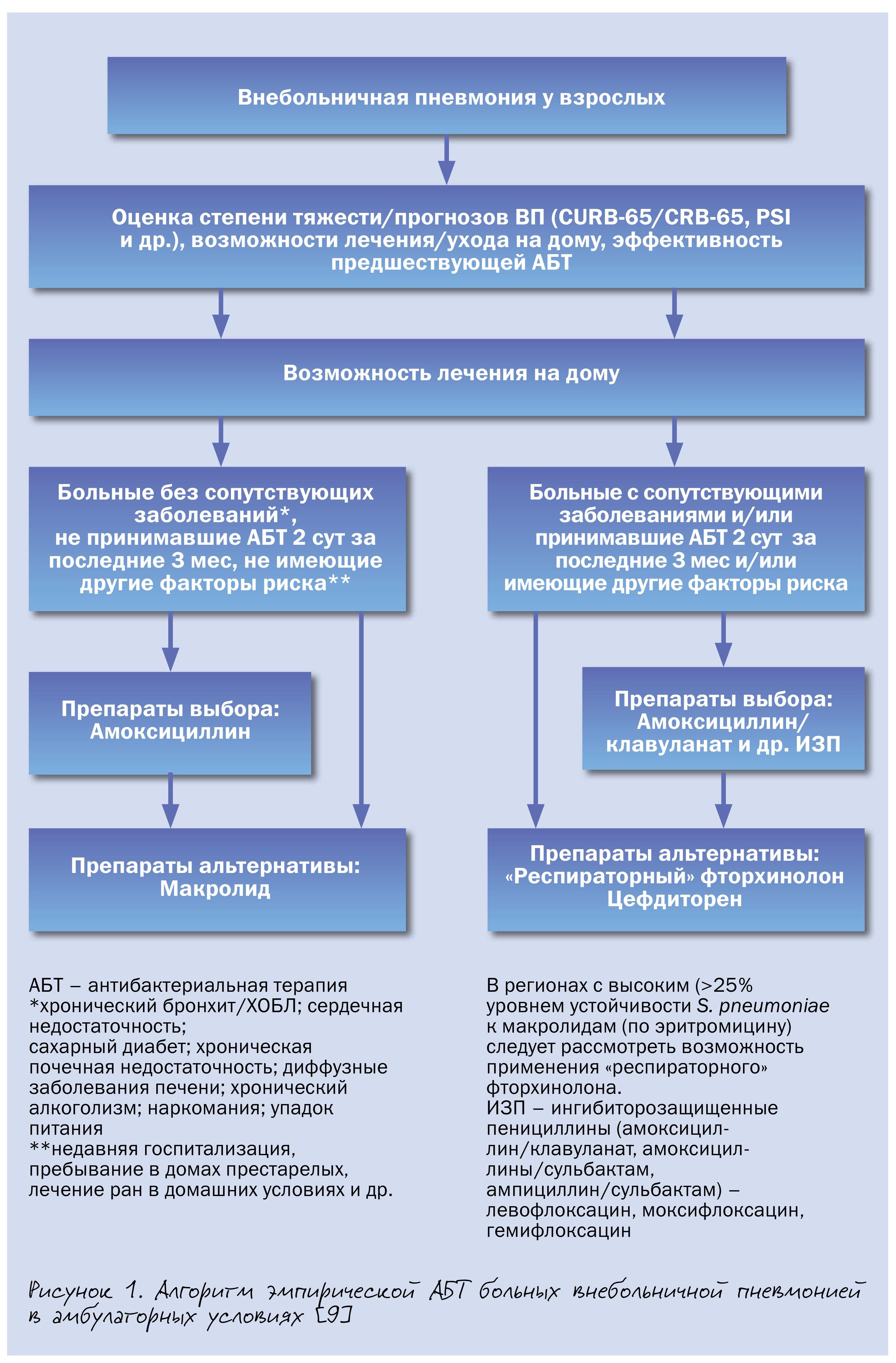
В данной клинической ситуации антибиотиком выбора является амоксициллин, альтернативы – макролиды. Последнее объясняется быстрым и существенным ростом устойчивости S. pneumoniae к макролидам в РФ и, как следствие этого, риском клинических неудач. Макролиды применяют, когда невозможно назначить амоксициллин (индивидуальная непереносимость, анамнестические указания на аллергические реакции немедленного типа на прием β-лактамов), а также при ВП микоплазменной или хламидийной этиологии.
Во вторую группу включены больные внебольничной пневмонией с сопутствующими заболеваниями (ХОБЛ, сахарный диабет, хроническая сердечная недостаточность, хроническая болезнь почек со снижением скорости клубочковой фильтрации, цирроз печени, алкоголизм, наркомания, истощение) и/или принимавшими за последние 3 мес. антибиотики в течение ≥2 последовательных дней и/или имеющими иные факторы риска инфицирования редкими и/или полирезистентными возбудителями. Поскольку вероятность этиологической роли грамотрицательных бактерий (в т. ч. обладающих некоторыми механизмами вторичной лекарственной устойчивости) у этих больных возрастает, то в качестве антибиотиков выбора рекомендуются ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.), а альтернативы – «респираторные» фторхинолоны и цефдиторен.
Подобный подход, предполагающий применение фторхинолонов в качестве альтернативной терапии, является общепринятым и обусловлен необходимостью уменьшить селекцию лекарственноустойчивых штаммов пневмотропных возбудителей и возможность их использования при неэффективности АБТ первого ряда. Несмотря на определенную роль «атипичных» возбудителей в этиологии внебольничной пенвмонии у пациентов данной группы, рутинное назначение комбинации β-лактамного антибиотика и макролида не рекомендуется, так как на сегодняшний день не доказано, что такая стратегия улучшает исходы лечения при возможном увеличении риска нежелательных лекарственных реакций и селекции антибиотикорезистентности.
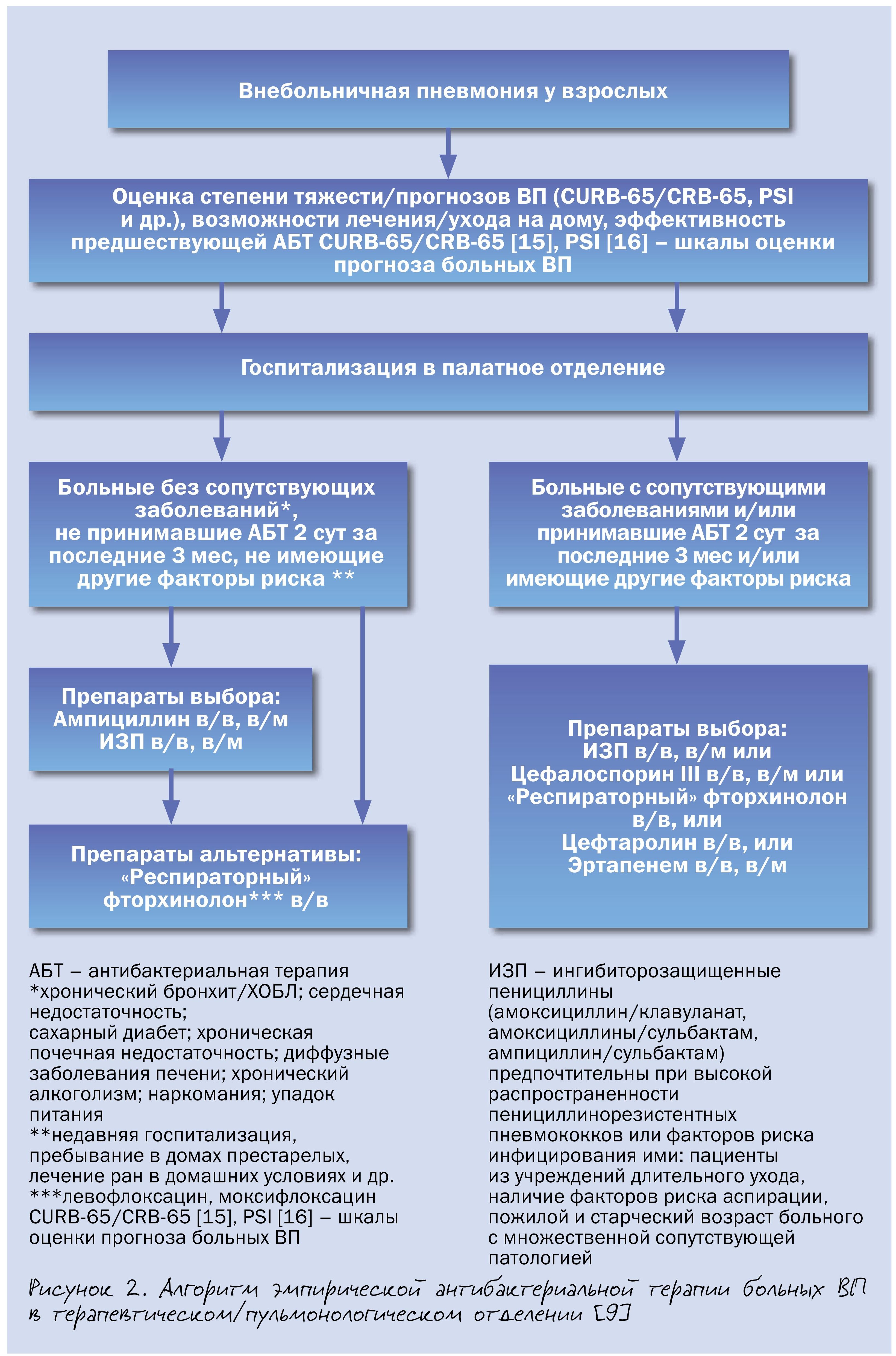
При госпитализации пациента с внебольничной пневмонией прежде всего необходимо решить вопрос о месте лечения – отделение общего профиля или ОИТ. Крайне важно быстро выявить признаки тяжелой внебольничной пневмонии (табл. 2), так как данные пациенты требуют неотложной помощи в условиях ОИТ.
У госпитализированных пациентов возможно применение широкого круга АБТ – ампициллина, ингибиторозащищенных пенициллинов (амоксициллин/клавуланат и др.), цефалоспоринов с высокой антипневмококковой активностью (цефотаксим, цефтриаксон, цефтаролин), эртапенема, «респираторных» фторхинолонов, демонстрирующих в целом сопоставимую эффективность. Стратификация больных аналогична таковой для амбулаторных пациентов.Антибиотиками выбора у госпитализированных больных с нетяжелой ВП без сопутствующих заболеваний и других факторов риска инфицирования редкими и/или полирезистентными возбудителями является ампициллин, альтернативными – ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.) и «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин).
Антибиотиками выбора у госпитализированных больных с нетяжелой ВП при сопутствующих заболеваниях и других факторов риска инфицирования редкими и/или полирезистентными возбудителями будут ингибиторозащищенные пенициллины (амоксициллин/клавуланат и др.), цефалоспорины III поколения (цефотаксим, цефтриаксон), «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин), а у отдельных категорий пациентов – цефтаролин и эртапенем. Несмотря на различия в спектре активности in vitro эффективность указанных режимов АБТ у данной категории пациентов сопоставима.
В регионах с высокой распространенностью пенициллинорезистентных пневмококков (ПРП), при наличии индивидуальных факторов риска инфицирования ПРП определенные преимущества может иметь цефтаролин. У пожилых пациентов с множественной сопутствующей патологией и высоким риском неблагоприятного прогноза, наличии факторов риска аспирации, обитателей домов престарелых более эффективно назначение эртапенема.
Имеющиеся доказательства превосходства комбинации «β-лактам + макролид» над монотерпией β-лактамами у госпитализированных больных ВП, полученные преимущественно в рамках обсервационных исследований, касаются, главным образом, тяжелого течения заболевания. Поэтому рутинное назначение комбинированной АБТ при нетяжелой ВП у госпитализированных пациентов нецелесообразно в связи с риском селекции антибиотикорезистентности (рис. 2).
Алгоритм эмпирической антибиотикотерапии больных с тяжелым течением внебольничной пневмонией представлен на рис. 3, однако детальное обсуждение вопросов ведения данной категории пациентов не входило в задачи настоящей статьи.
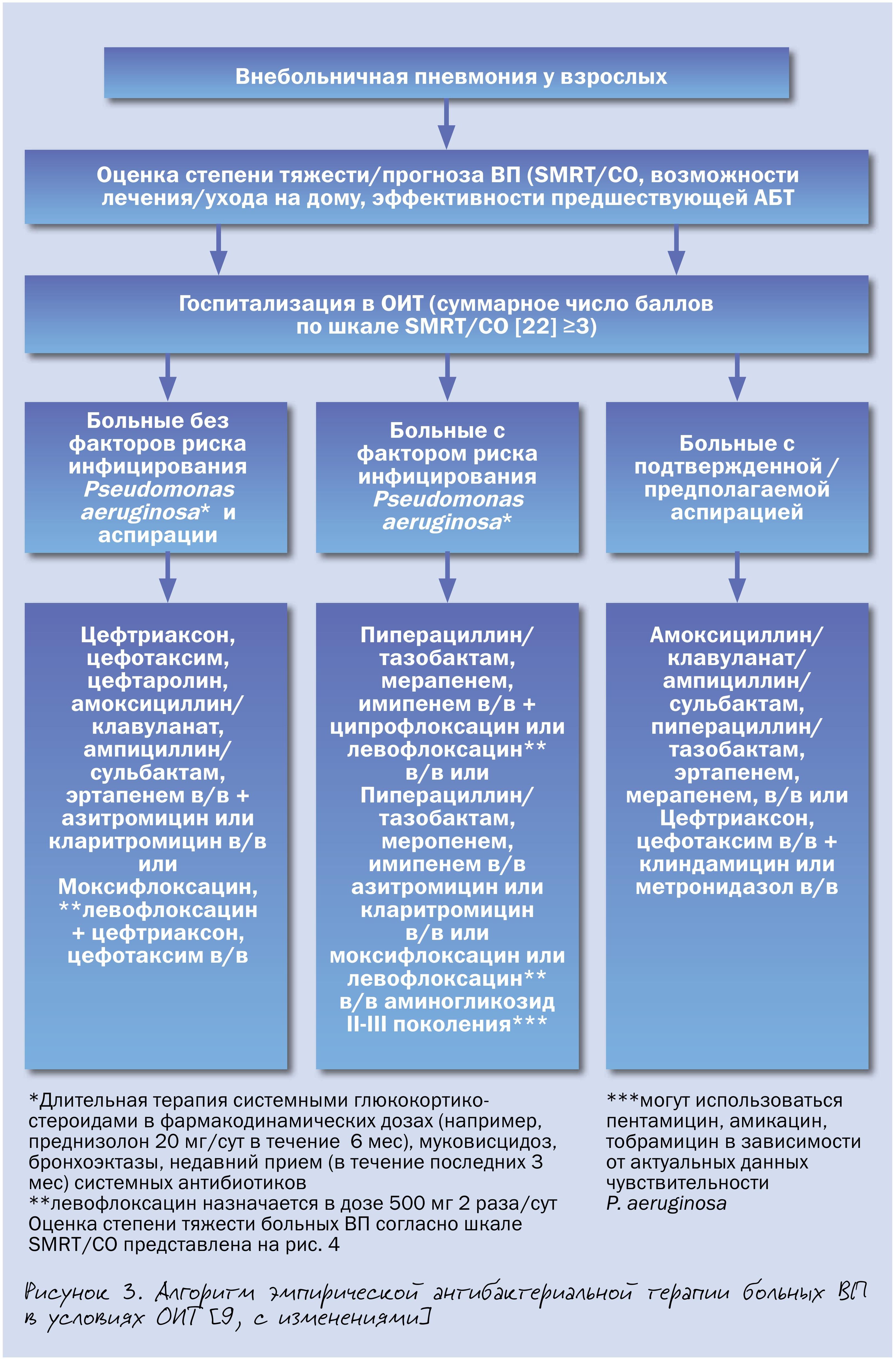
Алгоритмизация как определенная последовательность врачебных действий, представляющихся оптимальными, может оказаться весьма полезной, особенно на начальном этапе ведения больного ВП, когда врач испытывает известный информационный дефицит (этиология заболевания? чувствительность возбудителя ВП к антибиотикам? возможные осложнения ВП? «ответ» пациента на введение первых доз антибиотика? и др.).

Доказательством этому являются, в частности, многочисленные свидетельства того, что следование клиническим рекомендациям, приближающим нас к диагностическому и лечебному универсализму, минимизирует стоимость лечения, сокращает сроки госпитализации и сопровождается снижением летальности. Вместе с тем доступность диагностических и терапевтических алгоритмов не освобождает нас от «индивидуального прочтения» актуальной клинической ситуации в отдельно взятой стране или регионе с учетом локальной антибиотикорезистентности, географической вариабельности этиологии внебольничной пневмонии, сложившихся лечебных традиций (но не укоренившихся заблуждений), и особенностей организации медицинской помощи на амбулаторном и госпитальном этапах. Иными словами, широкая популяризация клинических рекомендаций или их отдельных элементов (включая диагностические и лечебные алгоритмы) вовсе не означает утраты врачом разумной автономии.Источники:
Книги:
Нозокомиальная пневмония у взрослых. 2-е издание
Презентация:
Внебольничная пневмония
Внебольничная пневмония
Внебольничная пневмония
Пневмонии
14.01.2020 | 21:11:58
Источник

