Врожденная пневмония мкб 10 код
Рубрика МКБ-10: P23.9
МКБ-10 / P00-P96 КЛАСС XVI Отдельные состояния, возникающие в перинатальном периоде / P20-P29 Дыхательные и сердечно-сосудистые нарушения, характерные для перинатального периода / P23 Врожденная пневмония
Определение и общие сведения[править]
Пневмония — острое инфекционное заболевание, вызванное микроорганизмами различной, преимущественно бактериальной, этиологии, характеризующееся очаговым поражением респираторных отделов легких, наличием внутриальвеолярной экссудации, выявляемой при физикальном или инструментальном исследовании, и симптомами системного воспаления различной степени выраженности.
В раннем неонатальном периоде пневмония проявляется картиной дыхательных расстройств, а клинические симптомы очагового и системного воспаления могут быть недостаточно выражены. По этой причине диагноз пневмонии считают верифицированным только в тех случаях, когда очаговое воспалительное поражение легких (нижних отделов дыхательных путей) подтверждено рентгенологически.
Поскольку, согласно определению экспертов ВОЗ, госпитальная пневмония — это заболевание, развившееся через 48 ч и позднее после госпитализации, то при выявлении пневмонии у новорожденных, находящихся в условиях акушерского или педиатрического стационара, в возрасте старше 2 сут жизни достаточно трудно провести дифференциальную диагностику между врожденной и нозокомиальной пневмонией.
Пневмонии, регистрируемые в перинатальном периоде, обозначают термином «врожденная пневмония». К ней же относят инфекционную пневмонию, развившуюся внутриутробно или при рождении. В зависимости от возбудителя они регистрируются под разными кодами.
Эпидемиология
Заболеваемость пневмонией составляет около 1% доношенных и около 10% недоношенных детей. У новорожденных, находящихся в отделении реанимации на ИВЛ, заболеваемость нозокомиальной пневмонией варьирует в широких пределах и может достигать 40-50%.
Классификация
В неонатологической практике пневмонию подразделяют в соответствии со следующими критериями:
• по времени возникновения — врожденная (внутриутробная) и неонатальная (госпитальная);
• по этиологическому принципу — вирусная, бактериальная, паразитарная, грибковая, смешанная;
• по распространенности процесса — очаговая, сегментарная, долевая, односторонняя, двусторонняя.
Этиология и патогенез[править]
Развитию пневмоний у новорожденных способствует большое количество неблагоприятных факторов, действующих на организм плода в антенатальном, интранатальном и постнатальном периодах. Пневмония у новорожденного может быть как первичным заболеванием, так и одним из очагов сепсиса или генерализованной вирусной инфекции. Непосредственными этиологическими агентами пневмонии бывают различные бактерии, вирусы, пневмоцисты, грибы и микоплазмы.
Среди бактериальных возбудителей врожденной пневмонии до середины 90-х годов прошлого века преобладали грамположительные микроорганизмы, в первую очередь стрептококк группы В. В последние десятилетия увеличился удельный вес пневмоний, вызванных грамотрицательными бактериями: клебсиеллой, кишечной палочкой, протеем. В последние годы вновь растет роль грамположительной микрофлоры.
Инфицирование тяжелобольных и глубоконедоношенных новорожденных после рождения может происходить в процессе лечения в условиях ОРИТН, особенно на фоне проведения ИВЛ. В этом случае возбудителем чаще всего бывает госпитальная микрофлора (Pseudomonas aeruginosa, Acinetobacter spp., Klebsiella pneumoniae, Enterobacter spp., грибы и др.). Заражение также происходит в результате нарушения санитарно-эпидемиологического режима персоналом при работе с венозными и артериальными линиями, обслуживании внешнего контура аппарата ИВЛ, недостаточно тщательном уходе за верхними дыхательными путями ребенка.
Патогенез
Инфекционный агент может попадать в легкие плода и новорожденного гематогенным путем (трансплацентарно) или при аспирации инфицированных околоплодных вод.
В постнатальном периоде заражение чаще происходит воздушно-капельным (бронхогенным) путем.
Однако неонатальные пневмонии возможны и при гематогенном распространении возбудителя при наличии у ребенка ЦВК.
В патогенезе пневмоний новорожденных большую роль играют несовершенство центральной регуляции дыхания, незрелость легочной ткани, недостаточная бактерицидная активность сурфактанта. Все это обусловливает повышенную восприимчивость недоношенных детей к развитию пневмонии.
Инфекционные (преимущественно бактериальные) агенты, поражая альвеолярную мембрану и интерстициальное пространство легких, вызывают развитие триады признаков: формирование гиалиновых мембран (особенно характерно для стрептококков группы В), гнойное воспаление и интерстициальный отек. В результате этих процессов развивается дыхательная недостаточность, сопровождающаяся гипоксемией, гиперкапнией и ацидозом. Тяжелые вторичные метаболические нарушения и выраженный инфекционный токсикоз при пневмонии у новорожденного нередко становятся причиной развития полиорганной недостаточности. В этом случае пневмонию рассматривают как симптом неонатального сепсиса.
Клинические проявления[править]
При врожденной пневмонии клиническая картина заболевания в первые сутки жизни трудноотличима от таковой при РДС (респираторный дистресс синдром). К одним из ранних косвенных признаков неонатальной пневмонии относят раннюю выраженную дисфункцию ЖКТ, проявляющуюся в значительном возрастании остаточного содержимого желудка, зачастую с примесью желчи. У доношенных детей, в случае раннего прикладывания к груди или начале ИВ (искусственное вскармливание), отмечают плохое сосание и срыгивания. Параллельно с развитием дыхательных расстройств появляются клинические признаки интоксикации в виде нарушения микроциркуляции, бледности или серости кожных покровов, увеличения размеров печении и селезенки, в ряде случаев развивается патологическая желтуха. В то же время, в отличие от более старших детей, кашель и лихорадка не характерны для новорожденных.
Врожденная пневмония неуточненная: Диагностика[править]
Диагноз врожденной пневмонии предполагают на основании соответствующей динамики состояния ребенка в периоде ранней неонатальной адаптации.
Для подтверждения диагноза используются две группы диагностических критериев: основные и вспомогательные.
Диагноз врожденной пневмонии может быть подтвержден, если выявлен хотя бы один основной или три (и более) вспомогательных диагностических признаков.
• Основные:
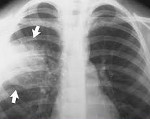
— очаговые и/или инфильтративные тени на рентгенограмме;
— высев из родовых путей матери и дыхательных путей или крови ребенка идентичной патогенной флоры;
— наличие пневмонии по данным патологоанатомического исследования, в случае смерти ребенка до конца 3-х суток жизни.
• Вспомогательные:
— лейкоцитоз выше 21х109/л, палочкоядерные — более 11% (анализ крови взят в первые сутки жизни);
— отрицательная динамика в анализе крови во 2-3-и сутки жизни;
— положительный прокальцитониновый тест в первые 48 ч жизни и/или повышение уровня С-реактивного белка в сыворотке крови в первые 72 ч жизни;
— наличие гнойной мокроты при первой интубации ребенка в 1-3-и сутки жизни (должно быть подтверждено результатом микроскопии мазка);
— усиление бронхо-сосудистого рисунка и/или локальное понижение прозрачности на рентгенограмме;
— жидкость в плевральных полостях по данным УЗИ или рентгенографического исследования с первых суток жизни (при отсутствии ГБН);
— увеличение печени в 1-е сутки жизни больше 2,5 см по правой среднеключичной линии (>2 см у детей с массой тела менее 1500 г) или пальпируемая селезенка (при отсутствии ГБН — Гемолитическая болезнь новорожденных);
— тромбоцитопения <150х109/л;
— наличие других гнойно-воспалительных заболеваний в первые трое суток жизни;
— воспалительные изменения в плаценте, обнаруженные при гистологическом исследовании.
Физикальное обследование
При осмотре обращают на себя внимание бледность и сероватый цвет кожных покровов, снижение рефлексов и мышечного тонуса.
При аускультации выслушиваются ослабление дыхания, разнокалиберные хрипы в легких; отмечают тахикардию и глухость тонов сердца.
Лабораторные исследования
При подозрении на пневмонию проводят следующие исследования:
• определение КОС (Кислотно-основное состояние) и газов крови (для выявления ацидоза, гипоксии, гиперкарбии);
• определение электролитов и глюкозы крови;
• клинический анализ крови с подсчетом тромбоцитов (при подозрении на врожденную пневмонию обязательно проведение анализа в динамике на первые и 2-е сутки жизни, с последующим регулярным контролем крови через 48-96 ч до момента стабилизации состояния);
• посев крови, бактериологическое исследование мазка из типичных локусов с определением чувствительности к антибиотикам;
• прокальцитониновый тест;
• С-реактивный белок.
Для уточнения характера воспалительного процесса необходимо как можно раньше сделать серию из нескольких рентгенограмм с интервалом 24-72 ч до момента стабилизации состояния. Для пневмонии характерны инфильтративные тени, они могут быть сливными или мелкими рассеянными; как правило, видно перибронхиальную инфильтрацию и усиление бронхо-сосудистого рисунка. При некоторых видах пневмонии (например, врожденная пневмония, вызванная стрептококком группы B) можно рассмотреть ретикулогранулярную или нодулярную сеть. Нельзя забывать, что в 20-30% случаев на рентгенограмме легких, выполненной до конца первых суток жизни, могут не выявляться характерные изменения.
Также рекомендуют контролировать состояние с помощью ряда дополнительных исследований.
• УЗИ головного мозга и внутренних органов.
• Допплерометрическое исследование центральной и регионарной гемодинамики в случаях проведения ИВЛ.
• Неинвазивный мониторинг основных показателей, особенно у больных, требующих респираторной поддержки: ЧСС, АД, температуры тела.
Дифференциальный диагноз[править]
Врожденная пневмония неуточненная: Лечение[править]
Цели лечения
Лечение пневмонии включает комплекс мероприятий, направленных на создание оптимальных условий выхаживания (комфортный микроклимат), коррекцию дыхательных нарушений, воздействие на этиологический фактор и ключевые звенья патогенеза.
Немедикаментозное лечение
Необходима респираторная терапия. При лечении пневмонии обычно придерживаются консервативной тактики. В большинстве случаев достаточно ингаляции увлажненной воздушно-кислородной смеси под контролем SpO2. Использование метода CPAP при пневмониях возможно. При прогрессировании дыхательных нарушений у детей с подтвержденным диагнозом пневмонии целесообразен перевод на ИВЛ. У доношенных новорожденных при прогрессирующих дыхательных нарушениях перевод на неинвазивную ИВЛ противопоказан.
Для проведения высокочастотной осцилляторной ИВЛ при пневмонии используют более низкие значения MAP из-за неоднородности изменений легочной ткани и опасности возникновения синдрома утечки воздуха. В фазу экссудации (при разрешении пневмонии) и потребности в частом размыкании контура для санации верхних дыхательных путей возможен ранний перевод на традиционную ИВЛ при достижении MAP менее 11 см вод.ст.
Медикаментозное лечение
При врожденной пневмонии неустановленной этиологии для проведения антибактериальной терапии используют комбинацию полусинтетических пенициллинов и аминогликозидов: ампициллина (внутривенно или внутримышечно, разовая доза составляет 25-50 мг каждые 8-12 ч) и нетилмицина (внутривенно 6 мг/кг 1 раз в сутки), курс — 7-10 сут.
Антибиотикотерапия нозокомиальных инфекций проводится индивидуально в соответствии с определяемой чувствительностью патогенных штаммов.
При пневмонии, вызванной метициллин-резистентными штаммами грамположительных кокков, назначают ванкомицин внутривенно 15 мг/кг однократно, затем по 10 мг/кг (разовая доза)
каждые 12 ч в первые 7 дней жизни и каждые 8 ч в возрасте старше 1 нед (вводится в растворе глюкозы в течение 1 ч).
В качестве альтернативы можно использовать линезолид внутривенно в течение 30-120 мин, разовая доза — 10 мг/кг, недоношенным детям в первые 7 дней жизни — каждые 12 ч, недоношенным старше 1 нед и доношенным, независимо от возраста, — каждые 8 ч.
В последние годы резко возросла роль метициллин-резистентных грамположительных штаммов стафилококков в возникновении нозокомиальной пневмонии и сепсиса.
В то же время стала отмечаться резистентность этих штаммов к ванкоцину (и даже к линезолиду). В связи с этим использование таких антистафилококковых антибиотиков, как даптомицин и фузидиевая кислота (внутривенная форма), может стать актуальным.
Курс антистафилококковых антибиотиков должен быть не менее 14 дней.
Назначение антибактериальной терапии при нозокомиальной пневмонии, вызванной грамотрицательными возбудителями должно осуществляться строго по чувствительности высеваемой флоры, с учетом концепции параллельного ущерба, а также миксконцепции. Назначение антибактериальной терапии должно согласовываться с микробиологом и клиническим фармакологом.
Профилактика[править]
Профилактика врожденной пневмонии заключается в своевременном выявлении и лечении инфекционных заболеваний у матери во время беременности. Успех в предотвращении нозокомиальной пневмонии зависит от строгого соблюдения санитарноэпидемиологического режима, использования одноразового расходного материала, оптимизации работы среднего медперсонала (не более 2 новорожденных в ОРИТН на 1 медицинскую сестру) и сокращения случаев необоснованного эмпирического назначения антибиотиков.
Прочее[править]
Прогноз
Смертность от врожденной пневмонии составляет 5-10%. При выздоровлении доношенных детей, перенесших врожденную бактериальную пневмонию, отдаленный прогноз, как правило, благоприятный. У глубоконедоношенных детей бактериальная и микоплазменная пневмония повышают риск развития БЛД (Бронхолегочная дисплазия). Смертность от нозокомиальной пневмонии зависит от преморбидного фона и степени морфофункциональной зрелости ребенка. Развитие госпитальной инфекции в условиях ОРИТН ухудшает исход и прогноз основного заболевания.
Источники (ссылки)[править]
Неонатология. Национальное руководство. Краткое издание [Электронный ресурс] / Под ред. Н.Н. Володина — М. : ГЭОТАР-Медиа, 2013. — https://www.rosmedlib.ru/book/ISBN9785970424438.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
Связанные заболевания и их лечение
Описания заболеваний
Стандарты мед. помощи
Содержание
- Описание
- Дополнительные факты
- Классификация
- Причины
- Симптомы
- Диагностика
- Лечение
- Прогноз
- Профилактика
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Внутрибольничная пневмония.

Внутрибольничная пневмония
Описание
Внутрибольничная пневмония. Легочная инфекция, развившаяся спустя двое и более суток после поступления больного в стационар, при отсутствии признаков заболевания на момент госпитализации. Проявления внутрибольничной пневмонии аналогичны таковым при других формах воспаления легких: лихорадка, кашель с мокротой, тахипноэ, лейкоцитоз, инфильтративные изменения в легких , однако могут быть слабо выраженными, стертыми. Диагноз основывается на клинических, физикальных, рентгенологических и лабораторных критериях. Лечение внутрибольничной пневмонии включает адекватную антибиотикотерапию, санацию дыхательных путей (лаваж, ингаляции, физиометоды), инфузионную терапию.
Дополнительные факты
Внутрибольничная (нозокомиальная, госпитальная) пневмония – приобретенная в стационаре инфекция нижних дыхательных путей, признаки которой развиваются не ранее 48 часов после поступления больного в лечебное учреждение. Нозокомиальная пневмония входит в тройку самых распространенных внутрибольничных инфекций, уступая по распространенности лишь раневым инфекциям и инфекциям мочевыводящих путей. Внутрибольничная пневмония развивается у 0,5-1% больных, проходящих лечение в стационарах, а у пациентов отделений реанимации и интенсивной терапии встречается в 5-10 раз чаще. Летальность при внутрибольничной пневмонии чрезвычайно высока – от 10-20% до 70-80% (в зависимости от вида возбудителя и тяжести фонового состояния пациента).

Внутрибольничная пневмония
Классификация
По срокам возникновения госпитальная инфекция подразделяется на раннюю и позднюю. Ранней считается внутрибольничная пневмония, возникшая в первые 5 суток после поступления в стационар. Как правило, она вызывается возбудителями, присутствовавшими в организме пациента еще до госпитализации (St аureus, St pneumoniae, H. Influenzae и тд представителями микрофлоры верхних дыхательных путей). Обычно эти возбудители проявляют чувствительность к традиционным антибиотикам, а сама пневмония протекает более благоприятно.
Поздняя внутрибольничная пневмония манифестирует через 5 и более дней стационарного лечения. Ее развитие обусловлено собственно госпитальными штаммами (метициллинрезистентным St аureus, Acinetobacter spp , P. Аeruginosa, Enterobacteriaceae и тд ), проявляющими высоковирулентные свойства и полирезистентность к противомикробным препаратам. Течение и прогноз поздней внутрибольничной пневмонии весьма серьезны.
С учетом причинных факторов выделяют 3 формы нозокомиальной инфекции дыхательных путей: вентилятор-ассоциированную, послеоперационную и аспирационную пневмонию. При этом довольно часто различные формы наслаиваются друг на друга, еще в большей степени утяжеляя течение внутрибольничной пневмонии и увеличивая риск летального исхода.
Причины
Основная роль в этиологии внутрибольничной пневмонии принадлежит грамотрицательной флоре (синегнойной палочке, клебсиелле, кишечной палочке, протею, серрациям и тд ) – эти бактерии обнаруживаются в секрете дыхательных путей в 50-70% случаев. У 15-30% пациентов ведущим возбудителем выступает метициллинрезистентный золотистый стафилококк. За счет различных приспособительных механизмов названные бактерии вырабатывают устойчивость к большинству известных антибактериальных средств. Анаэробы (бактериоды, фузобактерии и тд ) являются этиологическими агентами 10-30% внутрибольничных пневмоний. Примерно у 4% пациентов развивается легионеллезная пневмония – как правило, она протекает по типу массовых вспышек в стационарах, причиной которых служит контаминация легионеллами систем кондиционирования и водоснабжения.
Значительно реже, чем бактериальные пневмонии, диагностируются нозокомиальные инфекции нижних дыхательных путей, вызванные вирусами. Среди возбудителей внутрибольничных вирусных пневмоний ведущая роль принадлежит вирусам гриппа А и В, РС-вирусу, у больных с ослабленным иммунитетом – цитомегаловирусу.
Общими факторами риска инфекционных осложнений со стороны дыхательных путей служат длительная госпитализация, гипокинезия, бесконтрольная антибиотикотерапия, пожилой и старческий возраст. Существенное значение имеет тяжесть состояния больного, обусловленная сопутствующими ХНЗЛ, послеоперационным периодом, травмами, кровопотерей, шоком, иммуносупрессией, комой и пр. Способствовать колонизации нижних дыхательных путей микробной флорой могут медицинские манипуляции: эндотрахеальная интубация и реинтубация, трахеостомия, бронхоскопия, бронхография и пр. Основными путями попадания патогенной микрофлоры в дыхательные пути служат аспирация секрета ротоносоглотки или содержимого желудка, гематогенное распространение инфекции из отдаленных очагов.
Вентилятор-ассоциированная пневмония возникает у больных, находящихся на ИВЛ; при этом каждый день, проведенный на аппаратном дыхании, увеличивает риск развития внутрибольничной пневмонии на 1%. Послеоперационная, или застойная пневмония, развивается у обездвиженных больных, перенесших тяжелые оперативные вмешательства, главным образом, на грудной и брюшной полости. В этом случае фоном для развития легочной инфекции служит нарушение дренажной функции бронхов и гиповентиляция. Аспирационный механизм возникновения внутрибольничной пневмонии характерен для больных с цереброваскулярными расстройствами, у которых отмечаются нарушения кашлевого и глотательного рефлексов. В этом случае патогенное действие оказывают не только инфекционные агенты, но и агрессивный характер желудочного аспирата.
Симптомы
Особенностью течения внутрибольничной пневмонии является стертость симптомов, из-за чего распознавание легочной инфекции бывает затруднительным. В первую очередь, это объясняется общей тяжестью состояния больных, связанной с основным заболеванием, хирургическим вмешательством, пожилым возрастом, коматозным состоянием.
Боль в груди слева. Боль в грудной клетке. Влажный кашель. Высокая температура тела. Кашель. Лейкоцитоз. Ломота в теле. Мокрота. Одышка.
Диагностика
Полное диагностическое обследование при подозрении на внутрибольничную пневмонию строится на сочетании клинических, физикальных, инструментальных (рентгенография легких, КТ грудной клетки), лабораторных методов (ОАК, биохимический и газовый состав крови, бакпосев мокроты).
Для выставления соответствующего диагноза пульмонологи руководствуются рекомендуемыми критериями, включающими в себя: лихорадку выше 38,3°С, усиление бронхиальной секреции, гнойный характер мокроты или бронхиального секрета, кашель, тахипноэ, бронхиальное дыхание, влажные хрипы, инспираторную крепитацию. Факт внутрибольничной пневмонии подтверждается рентгенологическими признаками (появлением свежих инфильтратов в легочной ткани) и лабораторными данными (лейкоцитозом 12,0х109/л, палочкоядерным сдвигом 10%, артериальной гипоксемией Ра02.
С целью верификации вероятных возбудителей внутрибольничной пневмонии и определения антибиотикочувствительности производится микробиологическое исследование секрета трахеобронхиального дерева. Для этого используются не только образцы свободно откашливаемой мокроты, но и трахеальный аспират, промывные воды бронхов. Наряду с культуральным выделение возбудителя, широко применяется ПЦР-исследование.
Лечение
Сложность лечения внутрибольничной пневмонии заключается в полирезистентности возбудителей к противомикробным препаратам и тяжести общего состояния больных. Практически во всех случаях первоначальная антибиотикотерапия является эмпирической, т. Е. Начинается еще до микробиологической идентификации возбудителя. После установления этиологии внутрибольничной пневмонии может быть произведена замена препарата на более действенный в отношении выявленного микроорганизма.
Препаратами выбора при внутрибольничной пневмонии, вызванной E. Coli и K. Pneumoniae, служат цефалоспорины III-IV поколения, ингибиторзащищенные пенициллины, фторхинолоны. Синегнойная палочка чувствительна к сочетанию цефалоспоринов III-IV поколения (или карбапенемов) с аминогликозидами. Если госпитальные штаммы представлены St аureus, требуется назначение цефазолина, оксациллина, амоксициллина с клавулановой кислотой Для терапии аспергиллеза легких используется вориконазол или каспофунгин.
В начальном периоде предпочтителен внутривенный путь введения препарата, в дальнейшем при положительной динамике возможен переход на внутримышечные инъекции либо пероральный прием. Продолжительность курса антибиотикотерапии у пациентов с нозокомиальной пневмонией составляет 14-21 день. Оценка эффективности этиотропной терапии проводится по динамике клинических, лабораторных и рентгенологических показателей.
Кроме системной антибиотикотерапии, при внутрибольничной пневмонии важное внимание уделяется санации дыхательных путей: проведению бронхоальвеолярного лаважа, трахеальной аспирации, ингаляционной терапии. Больным показан активный двигательный режим: частая смена положения и присаживание в постели, ЛФК, дыхательные упражнения Дополнительно проводится дезинтоксикационная и симптоматическая терапия (инфузии растворов, введение и прием бронхолитиков, муколитиков, жаропонижающих препаратов). Для профилактики тромбозов глубоких вен назначается гепарин или ношение компрессионного трикотажа; с целью предупреждения стрессовых язв желудка используются Н2-блокаторы, ингибиторы протонной помпы. Пациентам с тяжелыми септическими проявлениями может быть показано введение внутривенных иммуноглобулинов.
Прогноз
Клиническими исходами внутрибольничной пневмонии могут быть разрешение, улучшение, неэффективность терапии, рецидив и летальный исход. Внутрибольничная пневмония является главной причиной смертности в структуре внутрибольничных инфекций. Это объясняется сложностью ее своевременной диагностики, особенно у пожилых, ослабленных больных, пациентов, пребывающих в коматозном состоянии.
Профилактика
Профилактика внутрибольничной пневмонии базируется на комплексе медицинских и эпидемиологических мероприятий: лечении сопутствующих очагов инфекции, соблюдении санитарно-гигиенического режима и инфекционного контроля в ЛПУ, предупреждении переноса возбудителей медперсоналом при проведении эндоскопических манипуляций. Чрезвычайно важна ранняя послеоперационная активизация пациентов, стимуляция откашливания мокроты; тяжелые больные нуждаются в адекватном туалете ротоглотки, постоянной аспирации трахеального секрета.
Основные медуслуги по стандартам лечения | ||
Клиники для лечения с лучшими ценами
|
Источник

